4.将氯气分别通入含有下列离子的溶液中,其中的离子不发生变化的是( )
| A. | SO42- | B. | Fe2+ | C. | S2- | D. | OH- |
3.下列对于“摩尔”的理解正确的是( )
| A. | 摩尔是国际科学界建议采用的一种物理量 | |
| B. | 摩尔是物质的量的单位,简称摩,符号为mol | |
| C. | 摩尔可以把物质的宏观数量与微观粒子的数量联系起来 | |
| D. | 国际上规定,12C碳-12原子所含有的碳原子数目的物质的量为1摩 |
1.离子晶体熔点的高低决定于阴、阳离子核间距离、离子电荷数和晶格能的大小,据所学知识判断KCl、NaCl、CaO、BaO四种晶体熔点的高低顺序是( )
| A. | KCl>NaCl>BaO>CaO | B. | NaCl>KCl>CaO>BaO | ||
| C. | CaO>BaO>NaCl>KCl | D. | CaO>BaO>KCl>NaCl |
20.元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体结构如图所示.下列说法错误的是( )

| A. | 晶体中每个Xn+周围有2个等距离且最近的N3- | |
| B. | Xn+中n=l | |
| C. | 该晶体中阳离子与阴离子个数比为3:1 | |
| D. | X元素的原子序数是19 |
19.下列有关叙述正确的是( )
| A. | 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 | |
| B. | 在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 | |
| C. | 只含有离子键的化合物才是离子化合物 | |
| D. | 在分子晶体中一定不存在离子键,而在离子晶体中可能存在共价键 |
18.下列描述正确的是( )
| A. | 3p2表示3p能级有两个轨道 | B. | 原子晶体中可能存在离子键 | ||
| C. | 分子晶体中一定存在共价键 | D. | sp2杂化轨道模型为 |
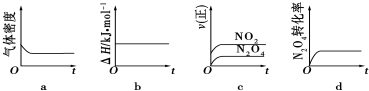
17.在密闭容器中进行反应:X(g)+3Y(g)?2Z(g),有关下列图象的说法不正确的是( )


| A. | 依据图甲可判断正反应为放热反应 | |
| B. | 在图乙中,虚线可表示使用了催化剂 | |
| C. | 若正反应的△H<0,图丙可表示升高温度使平衡向逆反应方向移动 | |
| D. | 由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的△H>0 |
16.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Fe2+、NO${\;}_{3}^{-}$、SO${\;}_{4}^{2-}$、Na+ | |
| B. | 水电离出的c(H+)=10-12mol•L-1的溶液中:Ca2+、K+、Cl-、HCO${\;}_{3}^{-}$ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的水溶液中:NH${\;}_{4}^{+}$、Al3+、NO${\;}_{3}^{-}$、Cl- | |
| D. | c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、SO${\;}_{4}^{2-}$、SCN- |
15.下列说法正确的是( )
0 153498 153506 153512 153516 153522 153524 153528 153534 153536 153542 153548 153552 153554 153558 153564 153566 153572 153576 153578 153582 153584 153588 153590 153592 153593 153594 153596 153597 153598 153600 153602 153606 153608 153612 153614 153618 153624 153626 153632 153636 153638 153642 153648 153654 153656 153662 153666 153668 153674 153678 153684 153692 203614
| A. | 因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 | |||||||||
| B. | 25℃、101kPa时,1mol S和2mol S的燃烧热不相等 | |||||||||
| C. | 通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能,例如:
| |||||||||
| D. | 任何化学反应都伴随着能量的变化 |