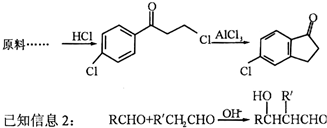
15.空气负离子[O2-(H2O)n]-对人体健康有着重要的生理意义,被誉为“空气维生素”,人吸入一定量的空气负离子,会减少某些疾病的发生.而“空调综合征”与室内缺少空气负离子有关.下列有关空气负离子的说法不正确的是( )
| A. | 具有很强的生物活性 | B. | 是一种十分稳定的化合物 | ||
| C. | 能增强人体抗病能力 | D. | 具有除尘、除臭和杀菌等作用 |
11.将一定量的锌与浓度为18.5mol/L的100mL浓硫酸充分反应后,锌完全溶解,同时生成26.88L标准状况下的气体,反应后测得溶液中氢离子浓度为1.0mol/L,则生成的气体的物质的量之比为( )
| A. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{1}$ | B. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{4}{1}$ | C. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{4}$ | D. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{3}{2}$ |
10.下列有关Fe2(SO4)3 溶液的叙述正确的是( )
| A. | 该溶液中,K+、Fe2+、I-、Br-可以大量共存 | |
| B. | 和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 | |
| C. | 1L0.1mol/L该溶液和足量的Cu充分反应,离子方程式为Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | 和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
9.两个体积相同的容器,一个盛有二氧化硫,一个盛有杂质为水蒸气的二氧化碳,在同温(120℃以上)同压(小于1个标准大气压)下,两容器内的气体一定相同的是( )
| A. | 质子质量 | B. | 质量 | C. | 密度 | D. | 原子总数 |
8.新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水.工业上常通过以下两步反应制备K2FeO4:①2FeCl3+10NaOH+3NaClO═2Na2FeO4+9NaCl+5H2O ②Na2FeO4+2KOH═K2FeO4+2NaOH,下列说法不正确的是( )
| A. | 反应①为氧化还原反应,反应②为复分解反应 | |
| B. | 反应①中NaClO是氧化剂 | |
| C. | Na2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒 | |
| D. | 若有2molFeCl3发生反应,转移电子的物质的量为6mol |
7.为了除去混入CO2中的SO2和O2,下列试剂的使用顺序正确的是( )
①饱和的Na2CO3溶液 ②饱和的NaHCO3溶液 ③浓硫酸 ④灼热的铜网 ⑤碱石灰.
0 153233 153241 153247 153251 153257 153259 153263 153269 153271 153277 153283 153287 153289 153293 153299 153301 153307 153311 153313 153317 153319 153323 153325 153327 153328 153329 153331 153332 153333 153335 153337 153341 153343 153347 153349 153353 153359 153361 153367 153371 153373 153377 153383 153389 153391 153397 153401 153403 153409 153413 153419 153427 203614
①饱和的Na2CO3溶液 ②饱和的NaHCO3溶液 ③浓硫酸 ④灼热的铜网 ⑤碱石灰.
| A. | ①③④ | B. | ②③④ | C. | ②④⑤ | D. | ③④⑤ |
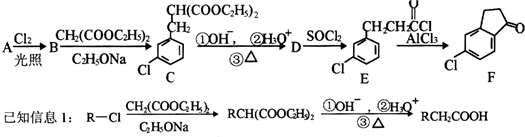
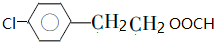 .
.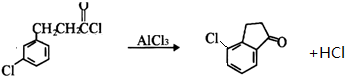 .
.