6.下列排列顺序正确的是:
①热稳定性:H2O>HF>H2S ②结合质子能力:OH->CH3COO->Cl-
③酸性:H3PO4>H2SO4>HClO4 ④原子半径:Na>Mg>O( )
①热稳定性:H2O>HF>H2S ②结合质子能力:OH->CH3COO->Cl-
③酸性:H3PO4>H2SO4>HClO4 ④原子半径:Na>Mg>O( )
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
5.下列有关说法中正确的是( )
| A. | 离子化合物熔沸点较高、共价化合物熔沸点较低 | |
| B. | 全部由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 离子半径:Na+>Mg2+>Al3+>F- | |
| D. | 熔点:金刚石>NaCl>CO2 |
4.卤族元素随着原子核电荷数的增加,下列叙述不正确的是( )
| A. | 原子半径依次增大 | B. | 单质的熔沸点逐渐升高 | ||
| C. | 卤离子的还原性逐渐减弱 | D. | 氢化物的热稳定性依次减弱 |
3.下列叙述正确的是( )
| A. | 合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 | |
| B. | 酸碱中和滴定时,锥形瓶需用待测液润洗2~3次,再加入待测液 | |
| C. | 将NO2、N2O4混合气体的体积压缩为原来的一半,则气体颜色加深 | |
| D. | 电解精炼铜过程中,阳极质量的减少与阴极质量的增加一定相等 |
2.在一密闭容器中,反应aA(g)+bB(g)?mC(s)+nD(g)达到平衡,保持温度不变,将容器体积减小为原来体积的$\frac{1}{2}$,达到新的平衡时,D的浓度是原来的1.7倍,下列说法正确的是( )
| A. | 物质B的转化率增大 | B. | 平衡向正反应方向移动 | ||
| C. | 物质A的体积分数增大 | D. | a+b<m+n |
1.恒温恒容的容器中,建立如下平衡:2A(g)?B(g),在相同条件下,若分别再向容器中通入一定量的A气体,重新达到平衡后,下列说法不正确的是( )
| A. | 平衡向右移动 | B. | A的体积分数比原平衡时小 | ||
| C. | A的转化率增大 | D. | 正反应速率增大,逆反应速率减小 |
20.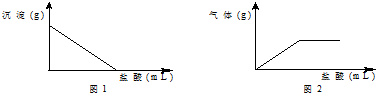 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )
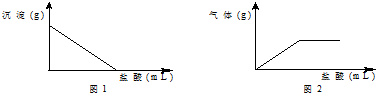 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )| A. | 取样溶于水,有白色沉淀产生,说明原白色固体中一定有Na2SO4和BaCl2 | |
| B. | 取样溶于水,静置后测得上层清液的pH>7,说明原白色固体中一定有NaOH | |
| C. | 取样溶于水,有白色沉淀产生,过滤后向沉淀中滴加盐酸,沉淀的量与加入盐酸体积的关系如图1所示,则原白色固体中无Na2SO4 | |
| D. | 取样溶于水,有白色沉淀产生,过滤后向沉淀中滴加盐酸,产生气体的量与加入盐酸体积的关系如图2所示,则该白色固体中无NaOH |
19.某原电池的结构如图所示,下列有关该原电池的说法不正确的是( )
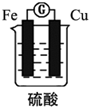

| A. | 该电池工作时电能转变为化学能 | B. | 铁片的质量变轻 | ||
| C. | 铜片上发生的反应2H++2e-=H2↑ | D. | SO42-向铁片移动 |
17.下列反应中的氨与反应4NH3+5O2═4NO+6H2O中的氨作用相同的是( )
0 153214 153222 153228 153232 153238 153240 153244 153250 153252 153258 153264 153268 153270 153274 153280 153282 153288 153292 153294 153298 153300 153304 153306 153308 153309 153310 153312 153313 153314 153316 153318 153322 153324 153328 153330 153334 153340 153342 153348 153352 153354 153358 153364 153370 153372 153378 153382 153384 153390 153394 153400 153408 203614
| A. | 2Na+2NH3═2NaNH2+H2↑ | B. | 2NH3+3CuO═3Cu+N2+3H2O | ||
| C. | NH3+HNO3═NH4NO3 | D. | 3SiH4+4NH3═Si3N4+12H2 |