1.若4.8g某金属与足量盐酸充分反应,放出4.48L(标准状况)H2,则该金属是( )
| A. | Al | B. | Mg | C. | Fe | D. | Zn |
19.常温常压下.甲烷与足量的氧气共60mL.点燃充分反应后.恢复到常温常压,剩余气体体积为24mL,则原混合气体中含甲烷( )
| A. | 25mL | B. | 17mL | C. | 18mL | D. | 25mL |
18.已知白磷跟O2可发生如下反应:P4+3O2═P4O6,P4+5O2═P4O10,某密闭容器中盛有31g白磷和1mol氧气,使之恰好完全反应后,所得到P4O6和P4O10的物质的量之比为( )
| A. | 1:1 | B. | 4:5 | C. | 4:3 | D. | 3:1 |
17.下列物质的分子中的所有原子一定在同一平面上的是( )
| A. | CH3-CH=CH2 | B. | CH2=CH2 | C. | C2H6 | D. | C6H6 |
16.下列对应关系不正确的是( )
| 选项 | A | B | C | D |
| 中心原子所在族 | ⅣA族 | ⅤA族 | ⅣA族 | ⅥA族 |
| 分子通式 | AB4 | AB3 | AB2 | AB2 |
| 立体构型 | 正四面体形 | 平面三角形 | 直线形 | V形 |
| A. | A | B. | B | C. | C | D. | D |
15.氨是化肥工业和基本有机化工的主要原料,合成氨工业因此成为基本无机化工之一.回答下列问题:
(1)如何获得廉价的氢气是合成氨工业中的重要课题,目前常用戊烷跟水蒸气反应的方法 获得氢气:
C5H12(g)+5H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$5CO(g)+11H2(g)
已知几个反应的能量变化如图所示,则上述反应的△H=c-5a-11bkJ•mol-1
 (2)合成氨的反应原理为:
(2)合成氨的反应原理为:
3H2(g)+N2(g) $?_{催化剂}^{高温高压}$2NH3(g)
现有甲、乙、丙3个固定容积为2L的密闭容器,在相同温度和催化剂条件下,按不同的反应物投入量进行合成氨反应,相关数据如下表所示:
①下列描述不能说明该反应已达到平衡状态的是a.(填序号);
a.容器内混合气体的密度保持不变
b.3v正(N2)═v逆(H2)
c.容器内混合气体的平均相对分子质量保持不变
②乙容器中的反应在20min后达到平衡,这段时间内NH3的平均反应速率v(NH3)=0.05mol•L-1•min-1,该温度下,反应的平衡常数K=5.33L2•mol-2(结果保留3位有效数字);
③分析上表中的数据,下列关系正确的是ac(填序号).
a.cl>c3 b.wl<w2 c.ρ2>ρ1>ρ3
(3)在合成氨工业中,为了提高反应物的利用率,除了要提供适宜的温度、压强和使用催化剂外,还要采取的措施是将产物混合气中的氨冷却分离后,剩余气体循环使用.
0 153163 153171 153177 153181 153187 153189 153193 153199 153201 153207 153213 153217 153219 153223 153229 153231 153237 153241 153243 153247 153249 153253 153255 153257 153258 153259 153261 153262 153263 153265 153267 153271 153273 153277 153279 153283 153289 153291 153297 153301 153303 153307 153313 153319 153321 153327 153331 153333 153339 153343 153349 153357 203614
(1)如何获得廉价的氢气是合成氨工业中的重要课题,目前常用戊烷跟水蒸气反应的方法 获得氢气:
C5H12(g)+5H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$5CO(g)+11H2(g)
已知几个反应的能量变化如图所示,则上述反应的△H=c-5a-11bkJ•mol-1
 (2)合成氨的反应原理为:
(2)合成氨的反应原理为:3H2(g)+N2(g) $?_{催化剂}^{高温高压}$2NH3(g)
现有甲、乙、丙3个固定容积为2L的密闭容器,在相同温度和催化剂条件下,按不同的反应物投入量进行合成氨反应,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2mol H2、2molN2 | 4mol H2、4molN2 | 2mol NH3 |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | C3 |
| 平衡时N2的体积分数 | w1 | W2 | W3 |
| 混合气体的密度(g•L-1) | ρ1 | ρ2 | ρ3 |
a.容器内混合气体的密度保持不变
b.3v正(N2)═v逆(H2)
c.容器内混合气体的平均相对分子质量保持不变
②乙容器中的反应在20min后达到平衡,这段时间内NH3的平均反应速率v(NH3)=0.05mol•L-1•min-1,该温度下,反应的平衡常数K=5.33L2•mol-2(结果保留3位有效数字);
③分析上表中的数据,下列关系正确的是ac(填序号).
a.cl>c3 b.wl<w2 c.ρ2>ρ1>ρ3
(3)在合成氨工业中,为了提高反应物的利用率,除了要提供适宜的温度、压强和使用催化剂外,还要采取的措施是将产物混合气中的氨冷却分离后,剩余气体循环使用.

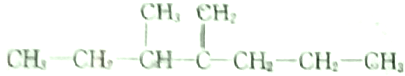 ,此烃名称为3-甲基-2-丙基-1-戊烯
,此烃名称为3-甲基-2-丙基-1-戊烯 ,可命名为1-甲基-3-乙基苯.
,可命名为1-甲基-3-乙基苯. 二氧化氯是一种黄绿色到橙黄色的气体,是国际上公认为安全、无毒的绿色消毒剂.回答下列问题:
二氧化氯是一种黄绿色到橙黄色的气体,是国际上公认为安全、无毒的绿色消毒剂.回答下列问题: .二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠和另一种氯的含氧酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-=ClO2-+ClO3-+H2O.
.二氧化氯还能溶于强碱溶液,该过程中发生反应生成等物质的量的氯酸钠和另一种氯的含氧酸盐,同时生成水,该反应的离子方程式为2ClO2+2OH-=ClO2-+ClO3-+H2O.