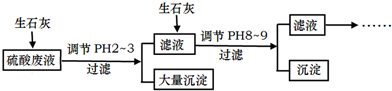
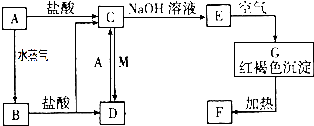
6.下列化学反应对应的离子方程式书写正确的是( )
| A. | 1-氯丙烷中加NaOH溶液后加热:CH3CH2CH2Cl+NaOH$→_{△}^{水}$CH3CH=CH2↑+NaCl+H2O | |
| B. | 将少量二氧化硫通入次氯酸钠溶液中:SO2+H2O+ClO-═SO42-+Cl-+2H+ | |
| C. | NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-═NH3•H2O | |
| D. | 用过量的氨水吸收烟道气中的SO2:SO2+2NH3•H2O═2NH4++SO32-+H2O |
4.用NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 0.1molCu和足量热浓硫酸反应可生成SO3分子数为0.1NA | |
| B. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| C. | 常温常压下,6.0g SiO2含有的SiO2分子数为0.1NA | |
| D. | 工业上将氨气与氧气在催化剂作用下发生氧化反应,若有标准状况下V L氨气完全反应,并转移n个电子,则阿伏加德罗常数NA可表示为:$\frac{22.4n}{5V}$ |
3.某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出来,要求每次只加一种溶液,滤出一种沉淀,所加溶液顺序正确的是( )
| A. | Na2CO3 NaCl NaOH | B. | NaOH NaCl Na2CO3 | ||
| C. | NaCl NaOH Na2CO3 | D. | NaCl Na2CO3 NaOH |
2.化学与人类社会的生产、生活有着密切联系.下列叙述中正确的是( )
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 不法商家制取的“地沟油”具有固定的熔沸点 | |
| C. | 钢铁制品和铜制品既能发生吸氧腐蚀又能发生析氢腐蚀 | |
| D. | 在家可用食醋代替CO2来增强漂白粉的漂白性 |
1.下列关于氯气、钠、镁的说法中,正确的是( )
| A. | 镁条燃烧可用泡沫灭火器灭火 | |
| B. | 工业上电解氯化钠、氯化镁溶液制取可以得到金属钠、镁 | |
| C. | 通常情况下,铁是银白色金属,硬度较大,可以被磁石吸引 | |
| D. | 铜能与氯化铁溶液反应,该反应可以用于印刷电路板的制作 |
20.实验设计是科学研究的重要步骤.下列叙述正确的是( )
| A. | Fe2O3固体可以用FeSO4溶液在蒸发皿中加热蒸干获得 | |
| B. | 可用碳酸氢铵溶液鉴别稀盐酸、氢氧化钠溶液、氯化铝溶液 | |
| C. | 用稀硝酸检验氢气还原氧化铜所生成的红色固体中含有氧化亚铜 | |
| D. | 测定相同条件下盐酸和磷酸溶液的pH,证明非金属性:Cl>P |
19.短周期元素W、X、Y、Z的原子序数依次增大,其中W的原子核中只有6个质子;X可与W形成两种常见的气体WX和WX2;Y是短周期元素中原子半径最大的元素;Z与Y形成的化合物的水溶液呈中性.下列叙述正确的是( )
| A. | Y位于第三周期,ⅦA族 | B. | 单质沸点:W>Y | ||
| C. | 气体氢化物稳定性:W>Z | D. | 离子半径:X<Y |
18.某无色溶液能溶解Al(OH)3,则此溶液中一定能大量共存的离子组是( )
0 153026 153034 153040 153044 153050 153052 153056 153062 153064 153070 153076 153080 153082 153086 153092 153094 153100 153104 153106 153110 153112 153116 153118 153120 153121 153122 153124 153125 153126 153128 153130 153134 153136 153140 153142 153146 153152 153154 153160 153164 153166 153170 153176 153182 153184 153190 153194 153196 153202 153206 153212 153220 203614
| A. | Fe2+、Cl-、Na+、NO3- | B. | Na+、Ba2+、Cl-、NO3- | ||
| C. | K+、Na+、NO3-、HCO3- | D. | Na+、K+、AlO2-、SO42- |