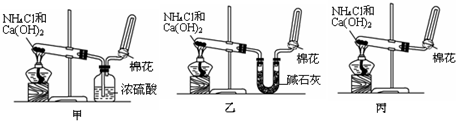
6.下列实验能达到实验目的且符合安全要求的是( )
| A. | 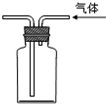 利用排空法收集CO2 | B. | 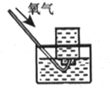 收集氧气 | ||
| C. | 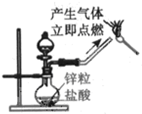 制备并检验氢气的可燃性 | D. | 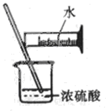 浓硫酸稀释 |
5.下列离子方程式书写正确的是( )
| A. | 氯化钙溶液中通入CO2气体 Ca2++CO2+H2O═CaCO3↓+2H+ | |
| B. | 以石墨作电极电解氯化铝溶液:2Cl${\;}^{_}$+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | Ca(ClO)2溶液中通人过量的SO2气体:Cl-+SO2+H2O═HClO+HSO${\;}_{3}^{-}$ | |
| D. | 向明矾溶液中加入氢氧化钡溶液至沉淀的质量最大:Al3++2SO${\;}_{4}^{2-}$+2Ba2++4OH-═2BaSO4+AlO${\;}_{2}^{-}$+H2O |
4.X、Y、Z、W分别为短周期主族元素,原子序数依次增加,Y、Z为同周期相邻的元素,且四种元素分布在所有短周期中.四种元素原子最外层电子数之和为16,且W为金属元素.下列有关叙述正确的是( )
| A. | 常见单质的沸点:X<Y<W | B. | 简单氢化物的热稳定性:Y>Z | ||
| C. | 简单离子的半径:W>Y>Z | D. | 四种元素只能形成两种离子化合物 |
3.(1)在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=13,则:
①该温度下,水的离子积常数Kw=10-13.
②该温度下,100mL 0.1mol/L的稀硫酸溶液中由水电离的c(OH-)=5×10-13mol/L.
(2)实验室用Na2SO3固体与70%的硫酸反应制取SO2气体时,可用NaOH溶液或Fe2(SO4)3溶液吸收多余的SO2气体.用Fe2(SO4)3溶液吸收多余的SO2气体,写出SO2与Fe2(SO4)3溶液反应的离子方程式SO2+2Fe3++2H2O=2Fe2++SO42-+4H+
(3)用Fe2(SO4)3溶液吸收SO2气体一段时间后,吸收液中一定存在的离子有H+、Fe2+、SO42-和极少量的OH-.某同学认为还可能存在其他离子,并提出假设进行实验探究.
①提出合理假设:
假设1:还存在HSO3-、SO32-;
假设2:还存在Fe3+;
假设3:HSO3-、SO32-、Fe3+都不存在
②设计实验方案
①该温度下,水的离子积常数Kw=10-13.
②该温度下,100mL 0.1mol/L的稀硫酸溶液中由水电离的c(OH-)=5×10-13mol/L.
(2)实验室用Na2SO3固体与70%的硫酸反应制取SO2气体时,可用NaOH溶液或Fe2(SO4)3溶液吸收多余的SO2气体.用Fe2(SO4)3溶液吸收多余的SO2气体,写出SO2与Fe2(SO4)3溶液反应的离子方程式SO2+2Fe3++2H2O=2Fe2++SO42-+4H+
(3)用Fe2(SO4)3溶液吸收SO2气体一段时间后,吸收液中一定存在的离子有H+、Fe2+、SO42-和极少量的OH-.某同学认为还可能存在其他离子,并提出假设进行实验探究.
①提出合理假设:
假设1:还存在HSO3-、SO32-;
假设2:还存在Fe3+;
假设3:HSO3-、SO32-、Fe3+都不存在
②设计实验方案
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,加稀硫酸酸化,然后再滴入几滴品红溶液; | 现象:品红不褪色 结论:假设1不成立; |
| 步骤2:另取少量吸收液于试管中, 滴入几滴KSCN溶液. | 现象:溶液变红 结论:假设2成立. |
2.X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构,下列说法正确的是( )
| A. | 原子最外层电子数:Z>Y>X | B. | 单质密度:Y>X>Z | ||
| C. | 离子半径:X2->Z->Y+ | D. | 原子序数:X>Z>Y |
1.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.其中Z所处的周期序数与族序数相等.下列说法不正确的是( )
| X | Y | Q | ||
| Z | W |
| A. | 形成简单离子的半径大小顺序:r(W)>r(Z)>r(Y) | |
| B. | 最简单气态氢化物的热稳定性:Y>X | |
| C. | Q的氢化物的水溶液可用于蚀刻玻璃 | |
| D. | X、Z的最高价氧化物均可与NaOH溶液反应 |
20.在MgSO4和Al2(SO4)3的混合溶液中,c(Al3+)=0.4mol•L-1,c(SO42-)=0.9mol•L-1,则c(Mg2+)为( )
| A. | 0.5 mol•L-1 | B. | 0.4 mol•L-1 | C. | 0.3 mol•L-1 | D. | 0.2 mol•L-1 |
18.二氧化硫能够使品红溶液褪色,表现了二氧化硫的( )
| A. | 氧化性 | B. | 还原性 | ||
| C. | 漂白性 | D. | 酸性氧化物的性质 |
17.有机物CH3CH2CH2CH3和CH3CH(CH3)2的关系是( )
0 153022 153030 153036 153040 153046 153048 153052 153058 153060 153066 153072 153076 153078 153082 153088 153090 153096 153100 153102 153106 153108 153112 153114 153116 153117 153118 153120 153121 153122 153124 153126 153130 153132 153136 153138 153142 153148 153150 153156 153160 153162 153166 153172 153178 153180 153186 153190 153192 153198 153202 153208 153216 203614
| A. | 互为同位素 | B. | 互为同系物 | C. | 互为同分异构体 | D. | 互为同种物质 |