13.水的电离平衡曲线如图所示,下列说法中,正确的( )
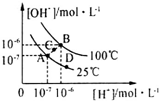

| A. | 图中A、B、D三点处Kw的大小关系:B>A>D | |
| B. | 25℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中c(NH4+)/c(NH3•H2O)的值逐渐减小 | |
| C. | 在25℃时,保持温度不变,在水中加人适量NH4Cl固体,体系可从A点变化到C点 | |
| D. | 100℃时,0.05mol•L-1 H2SO4溶液的pH≠1 |
12.下列各组性质比较中,正确的是( )
①失电子能力:K>Na>Li ②碱性:NaOH>Mg(OH)2>Al(OH)3 ③氧化性:F>Si>O ④稳定性:PH3<H2S<HCl.
①失电子能力:K>Na>Li ②碱性:NaOH>Mg(OH)2>Al(OH)3 ③氧化性:F>Si>O ④稳定性:PH3<H2S<HCl.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
8.下列离子反应方程式正确的是( )
| A. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O═H2SiO3↓+SO32- | |
| B. | 碳酸氢镁溶液中加入过量石灰水:Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+MgCO3↓ | |
| C. | 往FeCl3溶液中通入H2S气体:2Fe3++H2S═2Fe2++S↓+2H+ | |
| D. | 大苏打溶液中加入稀硫酸:S2O32-+2SO42-+6H+═4 SO2↑+3H2O |
7.NA代表阿伏加德罗常数的值.下列叙述正确的是(相对原子质量:Fe---56)( )
0 153015 153023 153029 153033 153039 153041 153045 153051 153053 153059 153065 153069 153071 153075 153081 153083 153089 153093 153095 153099 153101 153105 153107 153109 153110 153111 153113 153114 153115 153117 153119 153123 153125 153129 153131 153135 153141 153143 153149 153153 153155 153159 153165 153171 153173 153179 153183 153185 153191 153195 153201 153209 203614
| A. | 钢铁发生析氢腐蚀时,0.56gFe反应 转移电子数为0.03NA | |
| B. | 1L 0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA | |
| C. | 1molH2O2分子中的非极性共价键 1NA | |
| D. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4 NA |
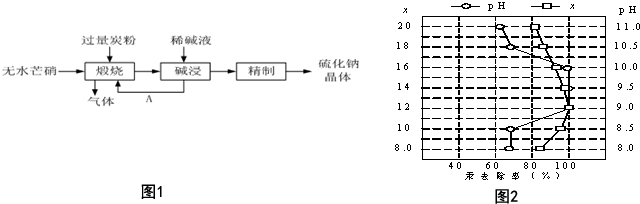
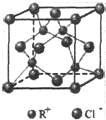 RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.
RCl常用作有机合成催化剂,并用于颜料,防腐等工业.R+中所有电子正好充满K、L、M三个电子层,它与Cl-形成的晶体结构如图所示.R的元素符号是Cu,每个Cl-周围最近的Cl-有12个.