14.化学与日常生活紧密相关,下列说法错误的是( )
| A. | 氮肥NH4NO3在重力撞击下可能发生爆炸 | |
| B. | 在食品袋中放入盛有硅胶的透气小袋,可防止食物受潮 | |
| C. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 | |
| D. | 碳酸氢钠可用来治疗胃酸过多 |
13.下列溶液中各组离子一定能够大量共存的是( )
| A. | 含有Fe3+的溶液:Na+、K+、SCN-、NO3- | |
| B. | 能使pH试纸显蓝色的溶液:K+、Ba2+、Cl-、Br- | |
| C. | 含有大量Al3+的溶液:Na+、Cl-、CO32-、OH- | |
| D. | 能使淀粉KI试纸显蓝色的溶液:K+、SO42-、Fe2+、NH4+ |
12.下列实验中的分离方法与对应原理均正确的是( )
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离溴水中的溴 | 乙醇萃取 | 溴在乙醇中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去乙烷中的乙烯 | 酸性高锰酸钾液体、洗气 | 乙烯可以用碱性高锰酸钾溶液除去氯化钠在水中的溶解度很大 |
| D | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
| A. | A | B. | B | C. | C | D. | D |
11.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 17g NH3和18 g H2O中含有的电子数均为10NA | |
| B. | 2 L 1.5 mol•L-1醋酸溶液中含有的CH3COO-数为3NA | |
| C. | 标准状况下,5.6 L Cl2溶解于足量NaOH溶液中,转移的电子数为0.5NA | |
| D. | 恒压密闭容器中充入2 mol NO与1 mol NO2,容器中分子数为3NA |
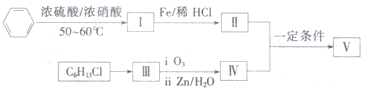
10.鲁米诺又名发光氨,广泛应用于刑事侦查、生物工程、化学示踪等领域.其制备方法之一如图: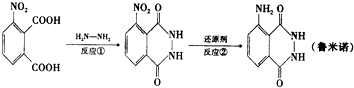
若反应②在催化剂作用下用H2还原,则制备1mol目标产物,理论上反应①与反应②生成水的质量比为( )

若反应②在催化剂作用下用H2还原,则制备1mol目标产物,理论上反应①与反应②生成水的质量比为( )
| A. | 1:2 | B. | 1:1 | C. | 2:1 | D. | 2:3 |
9.明末清初著名的科学家宋应星在其《天工开物》某条目下写道:“凡石灰经火焚炼为用.…百里内外,土中必生可燔石,石以青色为上,黄白次之.石必掩土内二三尺,掘取受燔,土面见风者不用.”其中的“可燔石”是指( )
| A. | 黏土 | B. | 纯碱 | C. | 石灰石 | D. | 熟石灰 |
8.下列说法正确的是( )
| A. | CO2的比例模型为 | |
| B. | H2O2的电子式是H:O:O:H | |
| C. | 甲烷的结构式为CH4 | |
| D. | 熔融状态下NaHSO4的电离方程式为NaHSO4=Na++HSO4- |
7.下列实验操作或事故处理正确的是( )
| A. | 金属钠着火时可用水扑灭 | |
| B. | 酒精灯着火时用湿抹布扑盖 | |
| C. | 蒸发结晶时,为得到更多晶体直接将溶液蒸干 | |
| D. | 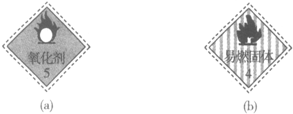 实验室可分别将贴有标志(a)和标志(b)的药品放在同一橱柜中 |
6.10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
(1)甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为HCO3-+H2O?H2CO3+OH-.
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3.
(2)丙同学认为甲、乙的判断都不充分.丙认为,只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙(填“甲”或“乙”)的判断正确.试剂X是B.
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言乙(填“甲”或“乙”)的判断是错误的,理由是常压下加热NaHCO3的水溶液,溶液的温度达不到150℃.
0 153001 153009 153015 153019 153025 153027 153031 153037 153039 153045 153051 153055 153057 153061 153067 153069 153075 153079 153081 153085 153087 153091 153093 153095 153096 153097 153099 153100 153101 153103 153105 153109 153111 153115 153117 153121 153127 153129 153135 153139 153141 153145 153151 153157 153159 153165 153169 153171 153177 153181 153187 153195 203614
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于(填“大于”或“小于”)NaHCO3.
(2)丙同学认为甲、乙的判断都不充分.丙认为,只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则乙(填“甲”或“乙”)的判断正确.试剂X是B.
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言乙(填“甲”或“乙”)的判断是错误的,理由是常压下加热NaHCO3的水溶液,溶液的温度达不到150℃.
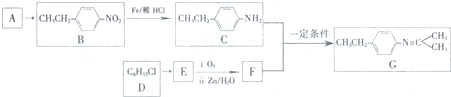
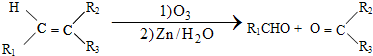
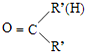 $\stackrel{一定条件}{→}$R-N=C
$\stackrel{一定条件}{→}$R-N=C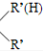 +H2O
+H2O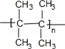 .
.
 .
.