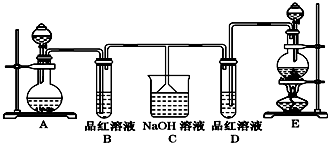
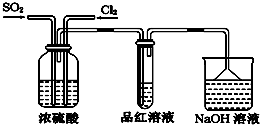
11.下列叙述正确的是( )
| A. | NaHCO3溶液中存在:c(OH-)=c(H+)+c(H2CO3) | |
| B. | 某二元弱酸强碱盐NaHA溶液中存在:c(Na+)+c(H+)=c(A2-)+c(HA-)+c(OH-) | |
| C. | CH3COONa和NaCl混合溶液中存在:c(Na+)=c(CH3COO-)+c(Cl-) | |
| D. | 常温下,10mL 0.02mol•L-1 HCl溶液与10mL 0.01mol•L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=7 |
9.下列说法正确的是( )
| A. | 向50 mL 1 mol•L-1的盐酸中加入烧碱,水的KW不变 | |
| B. | NH4Cl和NH3•H2O混合液中,二者对对方的平衡都起了抑制作用 | |
| C. | 有两种弱酸HX和HY且酸性HX>HY,则体积和浓度相同的NaX和NaY溶液中有c(Y-)>c(X-)>c(OH-)>c(H+) | |
| D. | 常温下0.1mol•L-1的HA溶液中c(OH-)/c(H+)=10-8,则0.01 mol•L-1HA溶液中c(H+)=1×10-4mol•L-1 |
8.下列物质中属于电解质是( )
| A. | 液态溴化氢 | B. | 蔗糖 | C. | 铝 | D. | 硝酸溶液 |
7.下列分子或离子在无色透明的溶液中能大量共存的是( )
| A. | Na+、H+、SO32-、H2O2 | B. | Al3+、Mg2+、OH-、CO32- | ||
| C. | K+、OH-、Cl-、NH3•H2O | D. | Ba2+、Fe3+、NO3-、Cl- |
6.下列各组离子,可以形成无色透明碱性溶液的是( )
| A. | K+、NH4+、OH-、NO3- | B. | Mg2+、Na+、AlO2-、OH- | ||
| C. | Na+、Ba2+、OH-、SO42- | D. | Cu2+、Al3+、SO42-、Cl- |
5.在我们的日常生活中出现了的“增铁酱油”,这里的铁应理解为( )
| A. | 铁的氢氧化物 | B. | 铁的氧化物 | C. | 铁元素 | D. | 铁屑 |
4.某学生只有下列仪器和用具:烧杯、试管、硬质玻璃管、圆底烧瓶、量筒、铁架台(带铁夹)、酒精灯、集气瓶、玻璃片、水槽、导气管、橡皮塞、橡皮管、100mL容量瓶、玻璃棒、药匙、火柴.从缺少仪器或用品的角度看,该学生能进行的实验操作是( )
| A. | 制蒸馏水 | |
| B. | 粗盐提纯 | |
| C. | 用氢气还原氧化铜 | |
| D. | 用氯化钠晶体配制100mL0.1mol•L-1的氯化钠溶液 |
2.在无色强酸性溶液中,下列各组离子能够大量共存的是( )
0 152976 152984 152990 152994 153000 153002 153006 153012 153014 153020 153026 153030 153032 153036 153042 153044 153050 153054 153056 153060 153062 153066 153068 153070 153071 153072 153074 153075 153076 153078 153080 153084 153086 153090 153092 153096 153102 153104 153110 153114 153116 153120 153126 153132 153134 153140 153144 153146 153152 153156 153162 153170 203614
| A. | Cl-、Na+、SO42-、Al3+ | B. | NH4+、HCO3-、Cl-、K+ | ||
| C. | K+、Ba2+、Cl-、SO42- | D. | Fe2+、Mg2+、NO3-、Cl- |
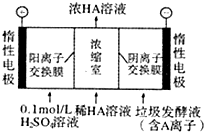 对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.