15.改变下列条件,一定能加快反应速率的是( )
| A. | 增加反应物的量 | B. | 增大压强 | C. | 加热 | D. | 减小压强 |
13.某工业废料中主要含有Al2O3、Co2O3•CoO、少量Fe3O4等金属氧化物(Co2O3•CoO不与强碱反应).实验室科技人员欲将之分离并制备相关物质,设计流程如下:
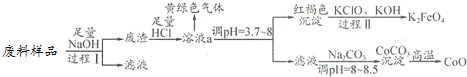
(1)过程Ⅰ中的操作名称是过滤,写出过程Ⅰ发生反应的化学方程式Al2O3+2NaOH═2NaAlO2+H2O.
(2)溶液a中含有金属离子有Co2+、Fe3+.
(3)溶液a中逸出的黄绿色气体是氯气,下列说法不正确的是①、④.
①氯气是有漂白性的酸性气体
②液氯和氯水均为液体,且都含有氯分子
③将氯气通入碱液时,氯气既是氧化剂,又是还原剂
④次氯酸见光易分解,说明次氯酸是弱酸
⑤向氯水中滴硝酸银溶液,有白色沉淀生成,说明氯水中含Cl-
(4)写出过程Ⅱ发生反应的离子方程式:2Fe(OH)3+3ClO-+4OH-═2FeO42-+5H2O+3Cl-.
高铁电池的总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH
则充电时阳极反应式为Fe(OH)3-3e-+5OH-═FeO42-+4H2O.
(5)Co可以形成CoC2O4•2H2O(M为183g/mol),5.49g该晶体在空气中加热,在不同温度下分别得到一种固体物质,其质量如表:
经测定,210℃~290℃过程中,产生的气体只有CO2,则此过程发生的化学反应方程式为:3CoC2O4+2O2$\frac{\underline{\;210℃~290℃\;}}{\;}$Co3O4+6CO2.

(1)过程Ⅰ中的操作名称是过滤,写出过程Ⅰ发生反应的化学方程式Al2O3+2NaOH═2NaAlO2+H2O.
(2)溶液a中含有金属离子有Co2+、Fe3+.
(3)溶液a中逸出的黄绿色气体是氯气,下列说法不正确的是①、④.
①氯气是有漂白性的酸性气体
②液氯和氯水均为液体,且都含有氯分子
③将氯气通入碱液时,氯气既是氧化剂,又是还原剂
④次氯酸见光易分解,说明次氯酸是弱酸
⑤向氯水中滴硝酸银溶液,有白色沉淀生成,说明氯水中含Cl-
(4)写出过程Ⅱ发生反应的离子方程式:2Fe(OH)3+3ClO-+4OH-═2FeO42-+5H2O+3Cl-.
高铁电池的总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH
则充电时阳极反应式为Fe(OH)3-3e-+5OH-═FeO42-+4H2O.
(5)Co可以形成CoC2O4•2H2O(M为183g/mol),5.49g该晶体在空气中加热,在不同温度下分别得到一种固体物质,其质量如表:
| 温度范围(℃) | 固体质量(g) |
| 150-210 | 4.41 |
| 290-320 | 2.41 |
| 890-920 | 2.25 |
10.化学用语是化学的重要工具.下列化学用语正确的是( )
| A. | 乙醇的分子式:C2H5OH | B. | F-的结构示意图: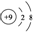 | ||
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | D. | +4价的硫元素:S4+ |
9.下列有关溶液的说法正确的是( )
| A. | 盐溶液是电解质 | |
| B. | 溶液和胶体的本质区别是有无丁达尔效应 | |
| C. | 可用NaOH溶液回收铝合金中的镁 | |
| D. | 小苏打溶液呈碱性的原因:HCO3-?OH-+CO2 |
8.下列有关酸性氧化物的说法正确的是( )
| A. | 均不能与酸反应 | B. | 均能与水直接化合生成酸 | ||
| C. | 能与碱反应生成盐和水 | D. | 不可能是金属氧化物 |
6.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
0 152919 152927 152933 152937 152943 152945 152949 152955 152957 152963 152969 152973 152975 152979 152985 152987 152993 152997 152999 153003 153005 153009 153011 153013 153014 153015 153017 153018 153019 153021 153023 153027 153029 153033 153035 153039 153045 153047 153053 153057 153059 153063 153069 153075 153077 153083 153087 153089 153095 153099 153105 153113 203614
| A. | 在常温常压下,2.24L SO2与O2混合气体中所含氧原子数为0.2NA | |
| B. | 标准状况下,20g D2O分子中所含中子数为10NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 50mL 12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
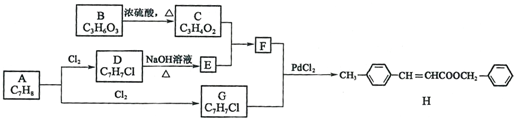
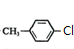 .
. .
.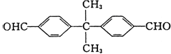 、
、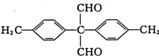 .
.