17.化学与生活、生产息息相关,下列说法不正确的是( )
| A. | 煤、石油、天然气属于化石能源,太阳能、氢能、风能、地热能、海洋能属于新能源 | |
| B. | 通常条件下能够自发进行的反应必须具备△H和△S均小于零 | |
| C. | 利用NaHCO3和Al2(SO4)3两种溶液来作泡沫灭火剂 | |
| D. | 测试和调控溶液的pH对工农业生产、科学研究及日常生活和医疗保健都有重要意义 |
16.标准状况下,把4.48L CO2通过一定量的过氧化钠固体后收集到3.36L气体,则这3.36L气体的质量是( )
| A. | 4.8g | B. | 5.4g | C. | 6.0g | D. | 6.6g |
15.下列有关物质的应用不恰当的是( )
| A. | 氧化铝可用作耐火材料 | B. | 氧化铁可用作红色油漆和涂料 | ||
| C. | 浓氨水可检验氯气管道漏气 | D. | 二氧化硫可用于食品增白 |
13.江苏有着丰富的海水资源,合理利用资源和保护环境是我省可持续发展的重要保证.
(1)海水经过处理后可以得到无水氯化镁,无水氯化镁是工业制取镁的原料.试写出由无水氯化镁制取金属镁的化学反应方程式MgCl2 $\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)某化工厂生产过程中会产生含有Cu2+和Pb2+的污水.排放前拟用沉淀法除去这两种离子,根据下列数据,你认为投入Na2S(选填“Na2S”或“NaOH”)效果更好.
(3)火力发电在江苏的能源利用中占较大比重,但是排放出的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如图所示: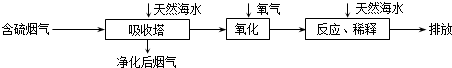
①天然海水的pH≈8海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子,试用离子方程式解释天然海水呈弱碱性的原因CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-(任写一个).
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示.

请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议:降低含硫烟气温度(或流速).
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,通入氧气氧化的化学原理是2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-(任写一个化学方程式或离子方程式).氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+).
(1)海水经过处理后可以得到无水氯化镁,无水氯化镁是工业制取镁的原料.试写出由无水氯化镁制取金属镁的化学反应方程式MgCl2 $\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)某化工厂生产过程中会产生含有Cu2+和Pb2+的污水.排放前拟用沉淀法除去这两种离子,根据下列数据,你认为投入Na2S(选填“Na2S”或“NaOH”)效果更好.
| 难溶电解质 | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |

①天然海水的pH≈8海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子,试用离子方程式解释天然海水呈弱碱性的原因CO32-+H2O?HCO3-+OH-或 HCO3-+H2O?H2CO3+OH-(任写一个).
②某研究小组为探究提高含硫烟气中SO2的吸收效率的措施,进行了天然海水吸收含硫烟气的模拟实验,实验结果如图所示.

请你根据图示实验结果,就如何提高一定浓度含硫烟气中SO2的吸收效率,提出一条合理化建议:降低含硫烟气温度(或流速).
③天然海水吸收了含硫烟气后会溶有H2SO3、HSO3-等分子或离子,通入氧气氧化的化学原理是2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-(任写一个化学方程式或离子方程式).氧化后的“海水”需要引入大量的天然海水与之混合后才能排放,该操作的主要目的是中和、稀释经氧气氧化后海水中生成的酸(H+).
12.下列说法不正确的是( )
| A. | 2H2表示的是2个氢气分子 | |
| B. | 4Cl-表示的是4个氯离子,每个氯离子带一个单位负电荷 | |
| C. | 3O表示的是3个氧元素 | |
| D. | 42Ca表示钙原子的质量数为42,质子数为20 |
11.在一密闭容器中存在如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析错误的是( )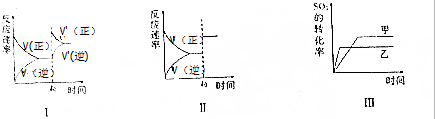

| A. | 图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 | |
| B. | 图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 | |
| C. | 图Ⅲ研究的是压强对化学平衡的影响,且乙的压强比甲高 | |
| D. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度比甲高 |
9.下列各组物质,前者逐滴滴加(或逐渐通入)到后者中直至过量,没有出现“先有白色沉淀,后来沉淀又完全消失”现象的是( )
| A. | 盐酸滴入Na[Al(OH)4]溶液中 | B. | CO2气体通入漂白粉溶液中 | ||
| C. | NaOH溶液滴入AlCl3溶液中 | D. | Ba(OH)2溶液滴入Al2(SO4)3溶液中 |
8.“绿色化学”中,最理想的“原子经济”是原子利用率为100%.下列反应类型能体现“原子经济”原则的事①取代反应②酯化反应③加成反应④置换反应⑤水解反应⑥化合反应( )
0 152897 152905 152911 152915 152921 152923 152927 152933 152935 152941 152947 152951 152953 152957 152963 152965 152971 152975 152977 152981 152983 152987 152989 152991 152992 152993 152995 152996 152997 152999 153001 153005 153007 153011 153013 153017 153023 153025 153031 153035 153037 153041 153047 153053 153055 153061 153065 153067 153073 153077 153083 153091 203614
| A. | ①④ | B. | ②⑤ | C. | ③⑥ | D. | ④⑤ |
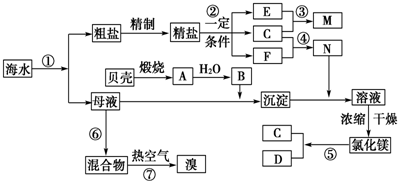 我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图:
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是某化工厂对海水资源综合利用的示意图: