7.设NA为阿伏加罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LCH4中含有氢原子数目为4NA | |
| B. | 1molNa2O2中含有的阴离子和阳离子的数目为2NA | |
| C. | 0.1mol/LCu(NO3)2溶液中含有的NO3-数目为0.2NA | |
| D. | 28gN2中所含的原子数目为NA |
6.下列有关物质的用途正确的是( )
| A. | NaHCO3可以用于治疗胃酸过多 | |
| B. | 浓硝酸具有强氧化性,因此浓硝酸可以作为漂白剂 | |
| C. | SiO2可以用于生产太阳能电池 | |
| D. | 在FeCl3饱和溶液里通入足量NH3可制取Fe(OH)3胶体 |
5.下列物质不属于混合物的是( )
| A. | 铝热剂 | B. | 水玻璃 | C. | 胆矾 | D. | 漂白粉 |
4.Cl2、SO2均能使品红溶液褪色,后者因为品红分子结构中的生色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物.其漂白原理可用下面的反应方程式表示:

下列说法正确的是( )

下列说法正确的是( )
| A. | 向品红溶液中同时通入Cl2、SO2,漂白效果会更好 | |
| B. | 加热可判断品红褪色是通入SO2还是通入Cl2引起的 | |
| C. | “无色化合物”分子中,19个碳原子都可能处在同一平面上 | |
| D. | 品红分子结构中,所有原子不可能处在同一平面上 |
3.下列离子方程式不正确的是( )
| A. | 乙酸与碳酸钠溶液反应:2 CH3COOH+CO32-→2CH3COO-+CO2↑+H2O | |
| B. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| C. | 醋酸溶液与新制氢氧化铜反应:2CH3COOH+Cu(OH)2→Cu2++2CH3COO-+2H2O | |
| D. | 乙醛溶液与足量的银氨溶液共热:CH3CHO+2[Ag(NH3)2]++2OH-$\stackrel{△}{→}$CH3COO-+NH4++2Ag↓+3NH3+H2O |
2.下列有机反应的化学方程式正确的是( )
| A. | CH3CH2Br+NaOH $→_{△}^{H_{2}O}$ CH2=CH2↑+NaBr+H2O | |
| B. | 2  +3Br2→2 +3Br2→2 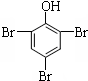 ↓ ↓ | |
| C. | nCH2=CH-CH3 $\stackrel{一定条件}{→}$ | |
| D. | 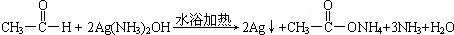 |
1.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.下列反应可制取K2FeO4:
2Fe(OH)3+3Cl2+10KOH $\frac{\underline{\;0~30℃\;}}{\;}$2K2FeO4+6KCl+8H2O
对于该反应,下列说法正确的是( )
2Fe(OH)3+3Cl2+10KOH $\frac{\underline{\;0~30℃\;}}{\;}$2K2FeO4+6KCl+8H2O
对于该反应,下列说法正确的是( )
| A. | 水是还原产物 | B. | Fe(OH)3发生还原反应 | ||
| C. | Cl2是氧化剂 | D. | 每生成1mol K2FeO4转移2mol电子 |
20.某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(1)氨基甲酸铵(NH2COONH4)分解反应是NH2COONH4(s)?2NH3(g)+CO2(g).
①某物质的标准摩尔生成焓是指在标准状态下由稳定单质生成1mol该物质时的反应焓变.
例如:CH3COOH的标准摩尔生成焓是指如下反应在标准状态下的焓变△H(CH3COOH)C(s)+O2(g)+H2(g)═CH3COOH(l)△H(CH3COOH)
已知NH2COONH4(s)、NH3(g)和CO2(g)的标准摩尔生成焓分别为△H1、△H2和△H3,则上述NH2COONH4分解反应的反应热△H=2△H2+△H3-△H1
②将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
实验测得不同温度下的平衡数据列于下表:
i.可以判断该分解反应已经达到化学平衡的是BC.
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
ii.根据表中数据,列式计算25.0℃时的分解平衡常数:1.6×10-8.(保留两位有效数字)
iii.取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.下列说法正确的是c.
a、恒温、压缩容器体积,再次达到平衡后,容器内的压强大于原平衡压强
b、恒温、增大容器体积,再次达到平衡后,容器内的c(CO2)小于原平衡时的浓度
c、固定活塞、升高温度,再次达到平衡后,容器内的压强大于原平衡时的压强.
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.
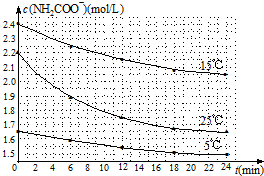
①计算25℃时,0~6min氨基甲酸铵水解反应的平均速率0.05mol/(L•min).
②根据图中信息,如何说明水解反应速率随温度升高而增大:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
(1)氨基甲酸铵(NH2COONH4)分解反应是NH2COONH4(s)?2NH3(g)+CO2(g).
①某物质的标准摩尔生成焓是指在标准状态下由稳定单质生成1mol该物质时的反应焓变.
例如:CH3COOH的标准摩尔生成焓是指如下反应在标准状态下的焓变△H(CH3COOH)C(s)+O2(g)+H2(g)═CH3COOH(l)△H(CH3COOH)
已知NH2COONH4(s)、NH3(g)和CO2(g)的标准摩尔生成焓分别为△H1、△H2和△H3,则上述NH2COONH4分解反应的反应热△H=2△H2+△H3-△H1
②将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
ii.根据表中数据,列式计算25.0℃时的分解平衡常数:1.6×10-8.(保留两位有效数字)
iii.取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.下列说法正确的是c.
a、恒温、压缩容器体积,再次达到平衡后,容器内的压强大于原平衡压强
b、恒温、增大容器体积,再次达到平衡后,容器内的c(CO2)小于原平衡时的浓度
c、固定活塞、升高温度,再次达到平衡后,容器内的压强大于原平衡时的压强.
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示.

①计算25℃时,0~6min氨基甲酸铵水解反应的平均速率0.05mol/(L•min).
②根据图中信息,如何说明水解反应速率随温度升高而增大:25℃反应物起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15℃大.
19.下列叙述正确的是( )
①同位素:1H、2H2、3H ②同素异形体:C60、金刚石、石墨 ③酸性氧化物:CO2、NO、SO3 ④混合物:水玻璃、水银、水煤气 ⑤电解质:明矾、冰醋酸、石膏 ⑥干冰、液氯、乙醇都是非电解质.
①同位素:1H、2H2、3H ②同素异形体:C60、金刚石、石墨 ③酸性氧化物:CO2、NO、SO3 ④混合物:水玻璃、水银、水煤气 ⑤电解质:明矾、冰醋酸、石膏 ⑥干冰、液氯、乙醇都是非电解质.
| A. | ②⑤ | B. | ②⑤⑥ | C. | ②④⑤⑥ | D. | ①②③④⑤⑥ |
18.下列分子中,所有原子都处在同一平面的是( )
0 152894 152902 152908 152912 152918 152920 152924 152930 152932 152938 152944 152948 152950 152954 152960 152962 152968 152972 152974 152978 152980 152984 152986 152988 152989 152990 152992 152993 152994 152996 152998 153002 153004 153008 153010 153014 153020 153022 153028 153032 153034 153038 153044 153050 153052 153058 153062 153064 153070 153074 153080 153088 203614
| A. | 环已烯 | B. | 苯 | C. | 丙烷 | D. | 丙炔 |