6.下列有关热化学方程式的叙述正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1,则氢气的标准燃烧热为-483.6kJ/mol | |
| B. | △H的数值与化学反应方程式的化学计量系数无关 | |
| C. | 含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则该反应的热化学方程式为:NaOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.4 kJ•mol-1 | |
| D. | 己知C(s)+O2(g)═CO2(g)△H1;C(g)+O2(g)═CO2(g)△H2,则△H1<△H2 |
4.下列说法正确的是( )
| A. | 同温同压下,H2 (g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不相同 | |
| B. | 用pH试纸测定新制氯水的pH | |
| C. | 已知:①2H2(g)+O2(g)═2H2O (g)△H1 ②2H2(g)+O2 (g)═2H2O(1)△H2,则△H1<△H2 | |
| D. | 在中和滴定实验中,用待测NaOH溶液润洗锥形瓶,测定结果将偏高 |
3.下列各组离子在指定的条件下一定能大量存在的是( )
| A. | 在pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl- | |
| B. | 常温下由水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Na+、Cl-、HCO3- | |
| C. | 有Fe3+存在的溶液中:CO32-、NH4+、SO42-、Cl- | |
| D. | 在能使石蕊试纸变蓝色的溶液中:Na+、K+、S2-、CO32- |
20.“分类”是一种思想方法,在化学发展中起到了重要的作用.下列说法正确的是( )
| A. | Na2O和Na2O2均能与H2O反应生成NaOH,故二者都是碱性氧化物 | |
| B. | 根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 | |
| C. | 根据水溶液能否导电将化合物分为电解质和非电解质 | |
| D. | 碱性氧化物一定是金属氧化物,酸性氧化物不一定是非金属氧化物 |
19.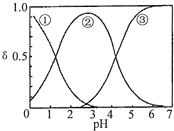 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )| A. | 曲线①代表的粒子是HC2O4- | |
| B. | 0.1 mol•L-1 NaHC2O4溶液中:c(Na+)=c(C2O42-)+c(H2C2O4)+c(HC2O4-) | |
| C. | pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 在一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(Ca2+)不变,c(C2O42-)将减小.(CaC2O4难溶于水) |
18.常温下,0.1mol/L CH3COONa溶液pH=9,则下列说法正确的是( )
| A. | 加入少量NaOH固体后溶液pH小于9 | |
| B. | 加水稀释,CH3COONa水解程度增大,c(OH-)增大 | |
| C. | 该溶液水电离出的c(OH-)═10-9 | |
| D. | CH3COOH在常温下Ka数值约为1×10-5 |
17.下列有关实验的说法正确的是( )
0 152847 152855 152861 152865 152871 152873 152877 152883 152885 152891 152897 152901 152903 152907 152913 152915 152921 152925 152927 152931 152933 152937 152939 152941 152942 152943 152945 152946 152947 152949 152951 152955 152957 152961 152963 152967 152973 152975 152981 152985 152987 152991 152997 153003 153005 153011 153015 153017 153023 153027 153033 153041 203614
| A. | 用pH试纸测双氧水的pH | |
| B. | 用酸式滴定管量取20.00 mL酸性K2Cr2O7溶液 | |
| C. | 用托盘天平称取 5.85 g NaCl晶体 | |
| D. | 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液 |
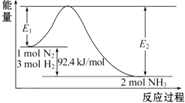 工业合成氨反应的能量变化如图所示.
工业合成氨反应的能量变化如图所示.