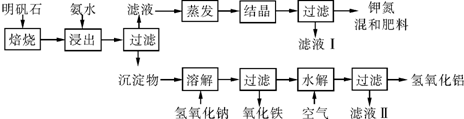
5.常温下,将体积均为10mL,pH均为11的 NaOH和CH3COONa溶液加水稀释,pH变化如图所示,下列结论正确的是( )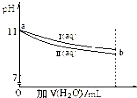

| A. | I 和 II 溶液中,离子种类数相同 | |
| B. | a 点处,I 溶液的浓度为 10-3mol?L-1 | |
| C. | a 点处,I、II 对水的电离平衡影响相同 | |
| D. | b 处的 I、II 溶液分别与盐酸反应,I 消耗 HCl 物质的量比 II 多 |
4.下列实验能达到预期实验目的是( )
| 实验 | 实验目的 |
| A.测定等物质的量浓度的 CH3COONa和Na2S溶液pH | 比较 CH3COOH和H2S的酸性强弱 |
B.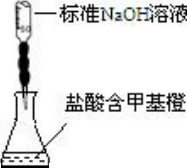 | 测定盐酸的浓度 |
C.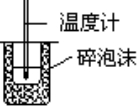 | 测定中和热 |
| D.先用酚酞,后用甲基橙作指示剂,用标准盐酸滴定0.1 mol/L的Na2CO3溶液 | 证明 CO32-水解分两步 |
| A. | A | B. | B | C. | C | D. | D |
3.已知 HF 酸性比 HCN 的酸性强.现有物质的量浓度和体积均相同的 NaF 和 NaCN 两种溶液,已知前者溶液中的离子数目为 n1,后者溶液中离子数目为 n2,下列关系正确的是( )
| A. | n1>n2 | B. | n1=n2 | C. | n2>n1 | D. | c(F-)<c(CN-) |
2.用食用白醋(醋酸浓度约1mol/L)进行下列实验,能证明醋酸为弱电解质的是( )
| A. | 白醋中滴入石蕊试液呈红色 | B. | 白醋加入豆浆中有沉淀产生 | ||
| C. | pH 试纸显示白醋的 pH 为 2~3 | D. | 蛋壳浸泡在白醋中有气体放出 |
1.下列说法正确的是( )
| A. | 氯水能导电,所以氯气是电解质 | |
| B. | CaCO3不溶于水,所以它是非电解质 | |
| C. | NaHCO3是强电解质,所以它的水溶液中不存在电离平衡 | |
| D. | 体积相同,c(OH-)相同的氨水和 NaOH 溶液被中和,前者消耗 HCl 多,所以NH3•H2O 是弱电解质 |
20.以下能正确表示电离方程式的是( )
| A. | BaSO4(s)?Ba2+(aq)+SO42-(aq) | B. | HClO=H++ClO- | ||
| C. | NaHSO3=Na++H++SO32- | D. | H2S+H2O?H3O++HS- |
19.氮化铝(AlN)具有耐高温.抗冲击.导热性好等优良性质,被广泛应用于电子工业.陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:
Al2O3+N2+3C$\stackrel{高温}{?}$ 2AlN+3CO下列叙述正确的是( )
0 152845 152853 152859 152863 152869 152871 152875 152881 152883 152889 152895 152899 152901 152905 152911 152913 152919 152923 152925 152929 152931 152935 152937 152939 152940 152941 152943 152944 152945 152947 152949 152953 152955 152959 152961 152965 152971 152973 152979 152983 152985 152989 152995 153001 153003 153009 153013 153015 153021 153025 153031 153039 203614
Al2O3+N2+3C$\stackrel{高温}{?}$ 2AlN+3CO下列叙述正确的是( )
| A. | 在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂 | |
| B. | 氮化铝是铝合金中的一种 | |
| C. | 上述反应中每生成2molAlN,N失去6mol电子 | |
| D. | 氮化铝中氮元素的化合价为-3 |
 2Ag(NH3)2+(aq)+2OH-(aq)△H=(2a-b)kJ?mol-1;
2Ag(NH3)2+(aq)+2OH-(aq)△H=(2a-b)kJ?mol-1;