5.下列说法正确的是( )
| A. | 需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 | |
| B. | 若 2C(s)+O2(g)=2CO(g)△H=-221.0 kJ/mol,则碳的燃烧热为110.5 kJ/mol | |
| C. |  如图可表示水分解过程中的能量变化 | |
| D. | 已知: Ⅰ:对于反应:H2(g)+Cl2(g)=2HCl (g)△H=-a kJ/mol, Ⅱ:  且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为(a+b+c)kJ |
4.已知化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
(1)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如下表:
①上述盐溶液中的阴离子,结合质子能力最强的是CO32-
②根据表中数据判断,浓度均为0.01mol•L-1的下列五种物质的溶液中,酸性最强的是D;(填编号,下同)将各溶液分别稀释100倍,pH变化最小的是C
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是CD(填编号).
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa═Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO
(2)CaCO3是一种难溶物质,其KSp=2.8×l0-9.现将浓度为2×l0-4 mol/L Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为5.6×10-5mol/L.
(1)常温下,浓度均为0.1mol•L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
②根据表中数据判断,浓度均为0.01mol•L-1的下列五种物质的溶液中,酸性最强的是D;(填编号,下同)将各溶液分别稀释100倍,pH变化最小的是C
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是CD(填编号).
A.CH3COOH+Na2CO3═NaHCO3+CH3COONa
B.CH3COOH+NaCN═CH3COONa+HCN
C.CO2+H2O+2NaClO═Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa═Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为2Cl2+CO32-+H2O=CO2↑+2Cl-+2HClO
(2)CaCO3是一种难溶物质,其KSp=2.8×l0-9.现将浓度为2×l0-4 mol/L Na2CO3溶液与CaCl2溶液等体积混合,则生成CaCO3沉淀所需CaCl2溶液的最小浓度为5.6×10-5mol/L.
2.下列物品中,都用到硅单质的是( )
①光导纤维 ②硅太阳能电池 ③玛瑙 ④计算机芯片.
①光导纤维 ②硅太阳能电池 ③玛瑙 ④计算机芯片.
| A. | ①③ | B. | ②④ | C. | ③④ | D. | ②③ |
1.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ | |
| B. | 向Na2SiO3溶液中通入过量CO2:SiO32ˉ+CO2+H2O═H2SiO3↓+CO32ˉ | |
| C. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O═AlO2ˉ+4NH4++2H2O | |
| D. | 向稀HNO3中滴加Na2SO3溶液:SO32ˉ+2H+═SO2↑+H2O |
20.下列属于电解质的是( )
| A. | 酒精 | B. | CO2 | C. | 盐酸 | D. | NaOH |
19.化学概念在逻辑上存在如下关系:
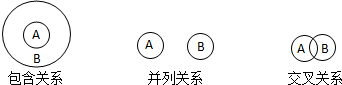
对下列概念的说法正确的是( )

对下列概念的说法正确的是( )
| A. | 纯净物与混合物属于包含关系 | |
| B. | 胶体与分散系属于交叉关系 | |
| C. | 置换反应与离子反应属于交叉关系 | |
| D. | 氧化还原反应与分解反应属于并列关系 |
18.下表是不同温度下水的离子积数据:
试回答以下问题:
(1)25℃下,某 Na2SO4 溶液中 c(SO42-)=5×10-4mol?L-1,取该溶液 1mL 加水稀释至10mL,则稀释后溶液中 c(Na+):c(OH-)=1000:1.
(2)在 t 2℃下,将 a mol?L-1CH3COOH 溶液与 b mol?L-1NaOH 溶液等体积混合反应后,溶液恰好呈中性,则该温度下 CH3COOH 的电离常数 Ka=$\frac{b×1{0}^{-6}}{a-b}$(用 a、b 表示).
| 温度/℃ | 25 | t 1 | t 2 |
| 水的离子积 KW | 1×10-14 | 1×10-13 | 1×10-12 |
(1)25℃下,某 Na2SO4 溶液中 c(SO42-)=5×10-4mol?L-1,取该溶液 1mL 加水稀释至10mL,则稀释后溶液中 c(Na+):c(OH-)=1000:1.
(2)在 t 2℃下,将 a mol?L-1CH3COOH 溶液与 b mol?L-1NaOH 溶液等体积混合反应后,溶液恰好呈中性,则该温度下 CH3COOH 的电离常数 Ka=$\frac{b×1{0}^{-6}}{a-b}$(用 a、b 表示).
17.下列溶液中,粒子浓度关系不正确的是( )
| A. | 在常温下,向 0.01mol?L-1 的 NH4HSO4 溶液中滴加 NaOH 溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH- )=c(H+) | |
| B. | 25℃时,在 0.1mol?L-1 的 NaHSO4 溶液中,c(H+)=c(OH- )+c(SO42-) | |
| C. | 浓度均为 0.1mol?L-1 的 HF 溶液和 KF 溶液等体积混合:c(F-)+c(HF)=0.2mol/L | |
| D. | 均为 0.1mol?L-1 的 Na2S 溶液和 NaHS 溶液等体积混合:2c(Na+)=3c(HS-)+3c(H2S)+3c(S2-) |
16.下列做法与盐类水解知识无关的是( )
0 152829 152837 152843 152847 152853 152855 152859 152865 152867 152873 152879 152883 152885 152889 152895 152897 152903 152907 152909 152913 152915 152919 152921 152923 152924 152925 152927 152928 152929 152931 152933 152937 152939 152943 152945 152949 152955 152957 152963 152967 152969 152973 152979 152985 152987 152993 152997 152999 153005 153009 153015 153023 203614
| A. | 实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 | |
| B. | 施肥时,草木灰(有效成分为 K2CO3)不能与碳酸氢铵混合使用 | |
| C. | Al2S不能用复分解反应的方法在溶液中制取,而只能用干法制备 | |
| D. | 配制 FeCl2溶液时常常要在溶液中加入少量铁粉 |
 工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法.
工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法.