20.有关物质的量的下列说法正确的是( )
| A. | 物质的量就是指物质的数量 | |
| B. | 硫酸的摩尔质量为98g | |
| C. | 标准状况下,0.5mol CCl4的体积为11.2L | |
| D. | 20.00 mL 0.5 mol/L的Ca(NO3)2溶液中NO3-的物质的量为0.02 mol |
19.下列说法不正确的是( )
| A. | 氢氧化铝可作胃酸的中和剂 | B. | 碳酸氢钠可作食品的膨松剂 | ||
| C. | 磁性氧化铁可作红色油漆和涂料 | D. | 钠钾合金可作原子反应堆的导热剂 |
18. 三氯化磷($\stackrel{+3}{P}$Cl3)和三氯氧磷(POCl3)是两种遇水会强烈水解的物质.PCl3是合成药物的重要化工原料;POCl3用于制取染料中间体,有机合成的氯化剂、催化剂和阻燃剂,还常用作半导体掺杂剂及光导纤维原料.
三氯化磷($\stackrel{+3}{P}$Cl3)和三氯氧磷(POCl3)是两种遇水会强烈水解的物质.PCl3是合成药物的重要化工原料;POCl3用于制取染料中间体,有机合成的氯化剂、催化剂和阻燃剂,还常用作半导体掺杂剂及光导纤维原料.
Ⅰ.白磷和Cl2化合制PCl3
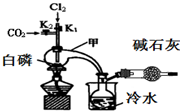
已知白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;PCl3遇O2会生成POCl3;POCl3能溶于PCl3.实验室制取PCl3的装置示意图和有关数据如下:
实验过程中要加入白磷、通入C02、通入Cl2、加热,实验时具体的操作顺序是:打开K2,使体系中充满CO2,再加入白磷,打开K1,通入氯气,再加热.
(1)干燥管中碱石灰的作用是吸收多余的氯气和空气中的水蒸气.
(2)PCl3强烈水解的产物是H3PO3和HCl,PC13遇水所得溶液中除OH-之外其它离子的浓度由大到小的顺序是c(H+)>c(Cl-)>c(H2PO3-)>c(HPO32-)(己知亚磷酸H3PO3是二元弱酸:H3PO3?H++H2PO3-,H2PO3-?H++HPO32-).
(3)实验制得的粗产品中常含有POCl3、PC15等,PC15先用白磷除去后,再用C方法除去PC13中的POCl3制备纯净的PCl3.
A.萃取 B.过滤 C.蒸馏 D.蒸发结晶
Ⅱ.氯化水解法生产POC13
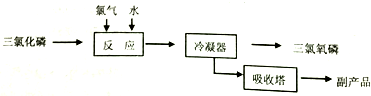
主要反应是:PC13+C12+H20═POC13+2HCl,流程如下:
(1)若将0.01mol POCl3加到水中水解,再与含2.4gNa0H的溶液混合充分反应,并配成1L的溶液,取出少量的溶液于试管中,再向其中逐滴加入0.010mol/L的AgNO3溶液,则先产生的沉淀是AgCl[已知Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10].
(2)通过下列方法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
A.取ag产品于锥形瓶中,加入足量Na0H 溶液,再加稀硝酸至酸性.
B.向锥形瓶中加入0.1000mol/L的AgN03溶液40.00mL,使Cl-完全沉淀.
C.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖.
D.加入指示剂,用cmol/LNH4SCN溶液滴定过量Ag+至终点,记下所用体积bmL.
己知:AgSCN是白色沉淀,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是B(填字母序号),滴定终点的现象为溶液由无色变为血红色,且30s不褪色.
A.FeCl2 B.NH4Fe(SO4)2 C.淀粉 D.甲基橙
②实验过程中加入硝基苯的目的是覆盖氯化银,防止沉淀转化生成AgSCN而导致数据不准确.如无此操作,所测Cl元素含量将会偏小(填“偏大”、“偏小”或“不变”).
③根据上面实验数据计算三氯氧磷产品中Cl元素的含量为$\frac{35.5(4-bc)}{1000a}$.
 三氯化磷($\stackrel{+3}{P}$Cl3)和三氯氧磷(POCl3)是两种遇水会强烈水解的物质.PCl3是合成药物的重要化工原料;POCl3用于制取染料中间体,有机合成的氯化剂、催化剂和阻燃剂,还常用作半导体掺杂剂及光导纤维原料.
三氯化磷($\stackrel{+3}{P}$Cl3)和三氯氧磷(POCl3)是两种遇水会强烈水解的物质.PCl3是合成药物的重要化工原料;POCl3用于制取染料中间体,有机合成的氯化剂、催化剂和阻燃剂,还常用作半导体掺杂剂及光导纤维原料.Ⅰ.白磷和Cl2化合制PCl3
已知白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;PCl3遇O2会生成POCl3;POCl3能溶于PCl3.实验室制取PCl3的装置示意图和有关数据如下:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 白磷 | 44.1 | 280.5 | 1.82 |
| PCl3 | -112 | 75.5 | 1.574 |
| POCl3 | 2 | 105.3 | 1.675 |
(1)干燥管中碱石灰的作用是吸收多余的氯气和空气中的水蒸气.
(2)PCl3强烈水解的产物是H3PO3和HCl,PC13遇水所得溶液中除OH-之外其它离子的浓度由大到小的顺序是c(H+)>c(Cl-)>c(H2PO3-)>c(HPO32-)(己知亚磷酸H3PO3是二元弱酸:H3PO3?H++H2PO3-,H2PO3-?H++HPO32-).
(3)实验制得的粗产品中常含有POCl3、PC15等,PC15先用白磷除去后,再用C方法除去PC13中的POCl3制备纯净的PCl3.
A.萃取 B.过滤 C.蒸馏 D.蒸发结晶
Ⅱ.氯化水解法生产POC13
主要反应是:PC13+C12+H20═POC13+2HCl,流程如下:

(1)若将0.01mol POCl3加到水中水解,再与含2.4gNa0H的溶液混合充分反应,并配成1L的溶液,取出少量的溶液于试管中,再向其中逐滴加入0.010mol/L的AgNO3溶液,则先产生的沉淀是AgCl[已知Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10].
(2)通过下列方法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
A.取ag产品于锥形瓶中,加入足量Na0H 溶液,再加稀硝酸至酸性.
B.向锥形瓶中加入0.1000mol/L的AgN03溶液40.00mL,使Cl-完全沉淀.
C.向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖.
D.加入指示剂,用cmol/LNH4SCN溶液滴定过量Ag+至终点,记下所用体积bmL.
己知:AgSCN是白色沉淀,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是B(填字母序号),滴定终点的现象为溶液由无色变为血红色,且30s不褪色.
A.FeCl2 B.NH4Fe(SO4)2 C.淀粉 D.甲基橙
②实验过程中加入硝基苯的目的是覆盖氯化银,防止沉淀转化生成AgSCN而导致数据不准确.如无此操作,所测Cl元素含量将会偏小(填“偏大”、“偏小”或“不变”).
③根据上面实验数据计算三氯氧磷产品中Cl元素的含量为$\frac{35.5(4-bc)}{1000a}$.
16.常温下,一种烷烃A和一种单烯烃B组成混合气体,A或B分子均最多只含有4个碳原子,且B分子的碳原子数比A 分子的多.将1升该混合气体充分燃烧,在同温同压下得到2.5升CO2气体.120℃时取1升该混合气体与9升氧气混和,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%.则A和B的分子式分别为( )
| A. | C2H6、C4H8 | B. | C2H6、C3H6 | C. | CH4、C4H8 | D. | CH4、C3H6 |
14.下列化学用语表达正确的是( )
①丙烷的球棍模型: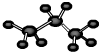
②丙烯的结构简式为:CH3CHCH2
③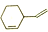 的化学式为C8H12
的化学式为C8H12
④一氯甲烷和二氯甲烷、乙烯和苯乙烯互为同系物
⑤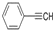 与C8H6互为同分异构体
与C8H6互为同分异构体
⑥石油是混合物,其分馏产品煤油为纯净物.
①丙烷的球棍模型:

②丙烯的结构简式为:CH3CHCH2
③
 的化学式为C8H12
的化学式为C8H12 ④一氯甲烷和二氯甲烷、乙烯和苯乙烯互为同系物
⑤
 与C8H6互为同分异构体
与C8H6互为同分异构体⑥石油是混合物,其分馏产品煤油为纯净物.
| A. | ①③④⑤ | B. | ①③ | C. | ②④⑥ | D. | ①② |
13.足量铜与一定量浓硝酸反应后过滤,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与3.36L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得溶液中加入1mol/L NaOH溶液至Cu2+恰好完全沉淀,将沉淀过滤、洗涤、干燥、灼烧后得到黑色固体,则所得黑色固体的质量是( )
| A. | 12g | B. | 16g | C. | 24g | D. | 48g |
12. 将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
 将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )
将一定量的CO2气体通入2L未知浓度的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体与HCl的物质的量的关系如图所示(忽略气体的溶解和HCl的挥发),下列说法不正确的是( )| A. | O点溶液中所含溶质的化学式为NaOH、Na2CO3 | |
| B. | 常温下,a点溶液显碱性 | |
| C. | 标准状况下,通入CO2的体积为4.48L | |
| D. | 原NaOH溶液的物质的量浓度为2.5mol/L |
11.标况下,将一盛有等体积NO、NO2的试管倒立在水槽中,充分反应后,下列叙述不正确的是(设试管中的溶质不往试管外扩散)( )
0 152808 152816 152822 152826 152832 152834 152838 152844 152846 152852 152858 152862 152864 152868 152874 152876 152882 152886 152888 152892 152894 152898 152900 152902 152903 152904 152906 152907 152908 152910 152912 152916 152918 152922 152924 152928 152934 152936 152942 152946 152948 152952 152958 152964 152966 152972 152976 152978 152984 152988 152994 153002 203614
| A. | 此反应中水既不是氧化剂又不是还原剂 | |
| B. | 试管内溶液中溶质的物质的量浓度为$\frac{1}{22.4}$mol/L | |
| C. | 溶液体积占试管容积的三分之二 | |
| D. | 若将试管中的气体换为氯化氢或者氨气,则水充满试管 |

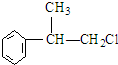 或
或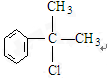 ;
;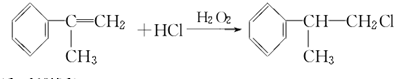 ;
;