7.已知甲醇的燃烧热数值为726.51kJ•mol-1.下列热化学方程式书写正确的是( )
| A. | CH4O+$\frac{3}{2}$O2═CO2+2H2O△H=-726.51 kJ•mol-1 | |
| B. | CH4O(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H=+726.51 kJ•mol-1 | |
| C. | 2CH4O(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1453.12 kJ•mol-1 | |
| D. | CH4O(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-726.51 kJ•mol-1 |
6.在pH=1的溶液中,下列各组离子能够大量共存的是( )
| A. | Fe3+、Mg2+、ClO-、SO42- | B. | Cu2+、Fe3+、NO3-、SO42- | ||
| C. | Na+、NH4+、CO32-、NO3- | D. | K+、HCO3-、Cl-、NH4+ |
5.已知:反应2A+3B=C+D在某段时间内,以A的浓度变化表示的反应速率为1mol/(L•min),则此段时间内,以C的浓度变化表示的化学反应速率为( )
| A. | 0.5 mol/(L•min) | B. | 2mol/(L•s) | C. | 2mol/(L•min) | D. | 3mol/(L•min) |
4.下列实验中,指定使用的仪器必须预先干燥的是( )
| A. | 喷泉实验中用于收集氨气的烧瓶 | |
| B. | 中和滴定中用的滴定管 | |
| C. | 配制一定物质的量浓度溶液实验用的容量瓶 | |
| D. | 排水法收集氧气实验用的集气瓶 |
3.在恒容的密闭容器中,下列能够判断可逆反应2A(g)+3B(g)?4C(g)+D(g) 已达到化学平衡状态的是( )
| A. | 单位时间内生成3n molB,同时消耗4n molC | |
| B. | 容器内压强不随时间变化 | |
| C. | 混合气体的密度不随时间变化 | |
| D. | B物质的百分含量不变 |
20.在众多的新能源中,氢能将会成为21世纪最理想的能源.
Ⅰ.已知101kPa、25℃时,1mol下列物质完全燃烧生成稳定状态化合物时放出的热量数
据如下:
(1)H2燃烧的热化学方程式是2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol.
(2)H2可以代替原煤和汽油作为新能源的依据是相同条件下,等质量的H2燃烧放出的热量大于原煤和汽油,产物无污染,可循环利用.
(3)工业上电解饱和食盐水的副产物之一是H2,反应的离子方程式是2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑.
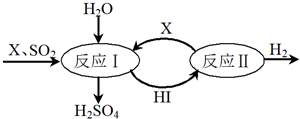
Ⅱ.如图所示,硫酸工业中产生的SO2通过下列过程既能制得H2SO4又能制得H2.
请回答:
(1)该过程可循环利用的物质是I2和HI(写化学式).
(2)该过程总反应的化学方程式是SO2+2H2O=H2SO4+H2.
(3)尾气中的SO2可用NaOH溶液吸收,同时可得含Na2SO3的样品,为测定样品中
Na2SO3的质量分数,甲同学设计实验如下(夹持及加热装置略):
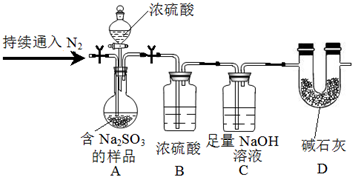
①装置B的作用是干燥SO2.
②测定样品中Na2SO3的质量分数所需的数据是含Na2SO3的样品质量、装置C通入SO2前后的质量.
Ⅰ.已知101kPa、25℃时,1mol下列物质完全燃烧生成稳定状态化合物时放出的热量数
据如下:
| 物质 | 氢气 | 原煤 (主要成份是C) | 汽油 (主要成份C8H18) |
| 热量(kJ) | 285.8 | 250.9 | 4910 |
(2)H2可以代替原煤和汽油作为新能源的依据是相同条件下,等质量的H2燃烧放出的热量大于原煤和汽油,产物无污染,可循环利用.
(3)工业上电解饱和食盐水的副产物之一是H2,反应的离子方程式是2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑.
Ⅱ.如图所示,硫酸工业中产生的SO2通过下列过程既能制得H2SO4又能制得H2.

请回答:
(1)该过程可循环利用的物质是I2和HI(写化学式).
(2)该过程总反应的化学方程式是SO2+2H2O=H2SO4+H2.
(3)尾气中的SO2可用NaOH溶液吸收,同时可得含Na2SO3的样品,为测定样品中
Na2SO3的质量分数,甲同学设计实验如下(夹持及加热装置略):

①装置B的作用是干燥SO2.
②测定样品中Na2SO3的质量分数所需的数据是含Na2SO3的样品质量、装置C通入SO2前后的质量.
19.醛或酮与氰化钠、氯化铵反应,生成α-氨基腈,经水解生成α-氨基酸盐,是制备α-氨基酸盐的一种简便方法,反应过程如下:

下列有关该反应说法不合理的是( )

下列有关该反应说法不合理的是( )
| A. | 反应①是加成反应 | |
| B. | 反应②需要在酸性环境中进行 | |
| C. | 反应②为碱性环境时,产物结构简式是 | |
| D. | 经过上述反应,苯乙醛可以制得 |
18.高铁酸钾(K2FeO4)是一种新型非氯高效消毒剂,主要用于饮用水处理.工业上可用如下方法制备:3ClO-+2Fe3++10OH-═2FeO42-+3Cl-+5H2O下列相关叙述不合理的是( )
0 152752 152760 152766 152770 152776 152778 152782 152788 152790 152796 152802 152806 152808 152812 152818 152820 152826 152830 152832 152836 152838 152842 152844 152846 152847 152848 152850 152851 152852 152854 152856 152860 152862 152866 152868 152872 152878 152880 152886 152890 152892 152896 152902 152908 152910 152916 152920 152922 152928 152932 152938 152946 203614
| A. | K2FeO4中铁元素的化合价是+6 | |
| B. | 制得1mol K2FeO4转移6 mol e- | |
| C. | K2FeO4做消毒剂的原因是其有强氧化性 | |
| D. | K2FeO4在消毒杀菌过程中还可以净水 |