7.常温下在下列条件时,可能大量共存的微粒组是( )
| 化学式 | 电离常数(25℃) |
| CH3COOH | K1=1.7×10-5 |
| HClO | K1=3.0×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
| A. | 如表提供的数据下:HClO、HCO3-、ClO-、CO32- | |
| B. | pH=3的溶液中:CO32-、Na+、SO42-、AlO2- | |
| C. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- | |
| D. | c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- |
6.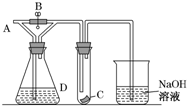 如图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( )
如图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( )
 如图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( )
如图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是( )| A. | 浓H2SO4 | B. | NaOH溶液 | C. | 浓盐酸 | D. | 饱和NaCl溶液 |
3.描述弱电解质电离情况可以用电离度和电离平衡常数表示,表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp).
表1
表2
请回答下面问题:
(1)表1所给的四种酸中,酸性最弱的是HCN(用化学式表示).下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是B(填序号).
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈中性(选填“酸性”、“中性”或“碱性”),溶液中各离子浓度大小关系是c(NH4+)=c(CH3COO-)>c(OH-)=c(H+).
(3)物质的量之比为1:1的NaCN和HCN的混合溶液,其pH>7,该溶液中电荷守恒等式为c(Na+)+c(H+)=c(CN-)+c(OH-).
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2).具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3.现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.01mol•L-1,则溶液中CO32-物质的量浓度应≥0.26mol•L-1.
表1
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3•H2O | 1.8×10-5 |
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1×10-10 |
| BaCO3 | 2.6×10-9 |
| CaSO4 | 7×10-5 |
| CaCO3 | 5×10-9 |
(1)表1所给的四种酸中,酸性最弱的是HCN(用化学式表示).下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是B(填序号).
A.升高温度 B.加水稀释 C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈中性(选填“酸性”、“中性”或“碱性”),溶液中各离子浓度大小关系是c(NH4+)=c(CH3COO-)>c(OH-)=c(H+).
(3)物质的量之比为1:1的NaCN和HCN的混合溶液,其pH>7,该溶液中电荷守恒等式为c(Na+)+c(H+)=c(CN-)+c(OH-).
(4)工业中常将BaSO4转化为BaCO3后,再将其制成各种可溶性的钡盐(如BaCl2).具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3.现有足量的BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.01mol•L-1,则溶液中CO32-物质的量浓度应≥0.26mol•L-1.
2.下列说法不正确的是( )
| A. | 苯环上有两个取代基的C9H12,其苯环上一氯代物的同分异构体(不考虑立体异构)共有10种 | |
| B. | 某只含有C、H、O、N的有机物的简易球棍模型如图所示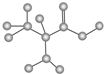 ,该有机物与CH3CH2CH2NO2互为同系物 ,该有机物与CH3CH2CH2NO2互为同系物 | |
| C. | 2,2-二甲基丙醇与 2-甲基丁醇互为同分异构体 | |
| D. | S诱抗素的分子结构如右图所示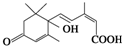 ,则该分子的分子式为C15H20O4 ,则该分子的分子式为C15H20O4 |
6.用氨水吸收排放的SO2将其转化为(NH4)2SO3,再氧化成(NH4)2SO4.25℃时0.1mol•L-1(NH4)2SO4.溶液的pH=5,其原因是NH4++H2O?NH3•H2O+H+(用离子方程式表示),若水解常数用Kh表示,则该温度下NH4+的水解常数Kn数值约为5×10-10.
已知25℃时
25℃时浓度均为0.1mol•L-1的四种溶液:①Na2S、②NaHS、③Na2SO3、④NaHSO3,pH由小到大的顺序是④NaHSO3<②NaHS<③Na2SO3<①Na2S(填序号).0.1mol•L-1的Na2S溶液中各离子浓度由大到小顺序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+).
已知25℃时
| 电解质 | Ka1 | Ka2 |
| H2S | 1.3×10-7 | 7.1×10-15 |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
5.在碱性溶液中能大量共存的离子组是( )
| A. | K+、Fe2+、NO3-、Cl- | B. | Na+、SO42-、Ba2+、H+ | ||
| C. | Na+、CO32-、Cl-、NO3- | D. | Al3+、K+、Cl-、SO42- |
4.关于氧化还原反应,下列说法正确的是( )
0 152750 152758 152764 152768 152774 152776 152780 152786 152788 152794 152800 152804 152806 152810 152816 152818 152824 152828 152830 152834 152836 152840 152842 152844 152845 152846 152848 152849 152850 152852 152854 152858 152860 152864 152866 152870 152876 152878 152884 152888 152890 152894 152900 152906 152908 152914 152918 152920 152926 152930 152936 152944 203614
| A. | 被还原的物质是氧化剂 | |
| B. | 还原剂被还原、氧化剂被氧化 | |
| C. | 得电子、化合价升高的物质是氧化剂 | |
| D. | 氧化剂反应后得到氧化产物 |



