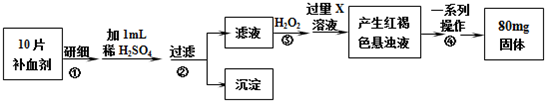
10.下列实验“操作和现象”与“结论”对应关系正确的是操作和现象结论( )
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4后,在试管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有砖红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液,红色褪去 | 使溶液褪色的气体是乙烯 |
| D | 向水玻璃溶液中通入足量CO2 后,产生白色浑浊 | 生成了硅酸沉淀 |
| A. | A | B. | B | C. | C | D. | D |
9.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 14g乙烯和丙烯的混合物中总原子数为3NA个 | |
| B. | 2mol/L的硫酸溶液中含有的H+离子数为4NA | |
| C. | 1mol 氯气与足量的铁反应后转移的电子数为3NA | |
| D. | 密闭容器中1molN2与3molH2在铂催化下充分反应,产物的分子数为2NA |
8.化学与社会、生产、生活密切相关,下列说法正确的是( )
0 152736 152744 152750 152754 152760 152762 152766 152772 152774 152780 152786 152790 152792 152796 152802 152804 152810 152814 152816 152820 152822 152826 152828 152830 152831 152832 152834 152835 152836 152838 152840 152844 152846 152850 152852 152856 152862 152864 152870 152874 152876 152880 152886 152892 152894 152900 152904 152906 152912 152916 152922 152930 203614
| A. | 二氧化硫可广泛用于食品的漂白 | |
| B. | 从海水提取物质都必须通过化学反应才能实现 | |
| C. | 葡萄糖可用于补钙药物的合成 | |
| D. | “地沟油”禁止食用,也不能用来制肥皂 |

 、
、 .
. 分子式相同,且能使氯化铁溶液显紫色的同分异构体还有11种(不考虑立体异构),其中核磁共振氢谱为4组峰,且峰的面积比为2:2:1:3的结构简式(写出其中任意两种)是
分子式相同,且能使氯化铁溶液显紫色的同分异构体还有11种(不考虑立体异构),其中核磁共振氢谱为4组峰,且峰的面积比为2:2:1:3的结构简式(写出其中任意两种)是 、
、 .
. .
.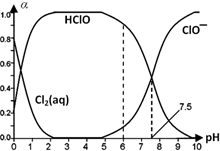 Cl2及其化合物在生产、生活中有广泛用途,回答下列问题.
Cl2及其化合物在生产、生活中有广泛用途,回答下列问题. HClO+H++Cl-或Cl2(aq)+H2O
HClO+H++Cl-或Cl2(aq)+H2O HClO+HCl、HClO
HClO+HCl、HClO H++ClO-.
H++ClO-.