3.磁流体是电子材料的新秀,它是由直径为纳米量级(1到10纳米之间)的磁性固体颗粒、基载液以及界面活性剂三者混合而成的分散系,既具有固体的磁性,又具有液体的流动性,下列关于纳米Fe3O4磁流体的说法中不正确的是( )
| A. | 纳米Fe3O4磁流体分散系属于溶液 | |
| B. | 纳米Fe3O4磁流体可以通过渗析法得到提纯 | |
| C. | 当一束可见光通过该磁流体时会出现光亮的通路 | |
| D. | 纳米Fe3O4磁流体比较稳定 |
2.某溶液中含有NH4+、SO32-、SiO32-、Br-、CO32-、Na+,向该溶液中通入过量的Cl2,下列判断不正确的是( )
| A. | 溶液中共发生了1个氧化还原反应 | |
| B. | 反应前后,溶液中离子浓度基本保持不变的有NH4+、Na+ | |
| C. | 有胶状物质生成 | |
| D. | 溶液颜色发生变化 |
1.若NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | NA个Fe(OH)3胶体粒子的质量为107g | |
| B. | 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA | |
| C. | 标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA | |
| D. | 5.6gFe与0.1mol Cl2完全反应,反应中转移的电子数为0.3NA |
20.下列有关化学实验安全问题的叙述中不正确的是( )
| A. | 闻化学药品的气味时都不能使鼻子凑近药品 | |
| B. | 点燃氢气前要检查纯度,以免发生爆炸 | |
| C. | 在盛O2集气瓶中进行铁丝燃烧实验时,事先在集气瓶底铺上一层沙子 | |
| D. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
18. 青蒿素是一种高效、速效抗疟药,是中医药献给世界的一份礼物.屠呦呦因在发现、研究青蒿素方面做出的杰出贡献而获得2015年诺贝尔医学奖.青蒿素分子结构如图,下列说法中正确的是( )
青蒿素是一种高效、速效抗疟药,是中医药献给世界的一份礼物.屠呦呦因在发现、研究青蒿素方面做出的杰出贡献而获得2015年诺贝尔医学奖.青蒿素分子结构如图,下列说法中正确的是( )
 青蒿素是一种高效、速效抗疟药,是中医药献给世界的一份礼物.屠呦呦因在发现、研究青蒿素方面做出的杰出贡献而获得2015年诺贝尔医学奖.青蒿素分子结构如图,下列说法中正确的是( )
青蒿素是一种高效、速效抗疟药,是中医药献给世界的一份礼物.屠呦呦因在发现、研究青蒿素方面做出的杰出贡献而获得2015年诺贝尔医学奖.青蒿素分子结构如图,下列说法中正确的是( )| A. | 青蒿素能与热的NaOH溶液反应 | |
| B. | 青蒿素的分子式为C15H21O5 | |
| C. | 青蒿素分子结构中只含有极性键 | |
| D. | 青蒿素能使酸性KMnO4溶液、溴的CCl4溶液分别褪色 |
16.氯元素是生产生活中常见的非金属元素.某同学探究Cl2及其化合物的性质.
(1)把Cl2通入水中,反应的化学方程式是Cl2+H2O?HCl+HClO.
(2)用氯水进行如下表实验:
①实验Ⅰ的现象说明,氯水具有的性质是酸性、强氧化性或漂白性.
②实验Ⅱ:a.ⅰ现象的白色沉淀是AgCl.
b.综合ⅰ、ⅱ现象,该同学推测实验Ⅱ发生的反应为:
Cl2+AgNO3+H2O=HNO3+AgCl↓+HClO(将反应补充完整)
③为探究实验Ⅰ中试纸褪色的原因及Ⅱ中另一种反应产物,该同学设计实验如下:
c.将少量稀硝酸点在蓝色石蕊试纸上,试纸变红未褪色;
d.…
上述实验d的方案是取实验Ⅱ中ⅱ的无色溶液,点在蓝色石蕊试纸上,试纸褪色.
(3)该同学查阅资料得知,最初,人们直接用氯气作漂白剂,但使用起来不方便,效果也不理想.经过多年的实验、改进,才有了今天常用的漂白粉.
①你认为“使用起来不方便,效果也不理想”的原因是氯气的溶解度不大,且生成的HClO不稳定,难保存.
②科研人员以氯气、石灰石、水为原料制取漂白粉,有关反应的化学方程式是:CaCO3═CaO+CO2↑,CaO+H2O=Ca(OH)2,2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O.
(1)把Cl2通入水中,反应的化学方程式是Cl2+H2O?HCl+HClO.
(2)用氯水进行如下表实验:
| 实验 | 操作 | 现象 |
| Ⅰ | 把氯水点在蓝色石蕊试纸上 | 试纸先变红后褪色 |
| Ⅱ | 向氯水中滴加足量AgNO3溶液,不断振荡 | ⅰ.有白色沉淀生成 ⅱ.稍后,溶液变为无色 |
②实验Ⅱ:a.ⅰ现象的白色沉淀是AgCl.
b.综合ⅰ、ⅱ现象,该同学推测实验Ⅱ发生的反应为:
Cl2+AgNO3+H2O=HNO3+AgCl↓+HClO(将反应补充完整)
③为探究实验Ⅰ中试纸褪色的原因及Ⅱ中另一种反应产物,该同学设计实验如下:
c.将少量稀硝酸点在蓝色石蕊试纸上,试纸变红未褪色;
d.…
上述实验d的方案是取实验Ⅱ中ⅱ的无色溶液,点在蓝色石蕊试纸上,试纸褪色.
(3)该同学查阅资料得知,最初,人们直接用氯气作漂白剂,但使用起来不方便,效果也不理想.经过多年的实验、改进,才有了今天常用的漂白粉.
①你认为“使用起来不方便,效果也不理想”的原因是氯气的溶解度不大,且生成的HClO不稳定,难保存.
②科研人员以氯气、石灰石、水为原料制取漂白粉,有关反应的化学方程式是:CaCO3═CaO+CO2↑,CaO+H2O=Ca(OH)2,2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O.
15.经检测某工厂的酸性废水中所含离子及其浓度如下表所示:
(1)c(H+)=0.01mol/L.
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4•7H2O).
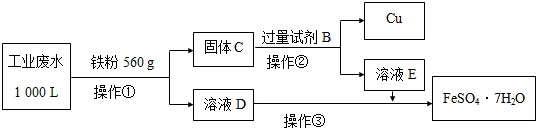
①工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+═Fe2++Cu、Fe+2Fe3+═3Fe2+、Fe+2H+═Fe2++H2↑.
②试剂B是H2SO4.
③操作③是蒸发浓缩、冷却结晶、过滤,最后用少量冷水洗涤晶体,在低温下干燥.
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是取少量D中溶液于试管中,滴加1滴KSCN溶液,不出现红色,说明废水中Fe3+除尽.
⑤获得的FeSO4•7H2O需密闭保存,原因是FeSO4有还原性,易被氧化(或FeSO4•7H2O失去结晶水).
⑥上述1000L废水经处理,可获得 FeSO4•7H2O的物质的量是12mol.
0 152735 152743 152749 152753 152759 152761 152765 152771 152773 152779 152785 152789 152791 152795 152801 152803 152809 152813 152815 152819 152821 152825 152827 152829 152830 152831 152833 152834 152835 152837 152839 152843 152845 152849 152851 152855 152861 152863 152869 152873 152875 152879 152885 152891 152893 152899 152903 152905 152911 152915 152921 152929 203614
| 离子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
| 浓度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4•7H2O).

①工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+═Fe2++Cu、Fe+2Fe3+═3Fe2+、Fe+2H+═Fe2++H2↑.
②试剂B是H2SO4.
③操作③是蒸发浓缩、冷却结晶、过滤,最后用少量冷水洗涤晶体,在低温下干燥.
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是取少量D中溶液于试管中,滴加1滴KSCN溶液,不出现红色,说明废水中Fe3+除尽.
⑤获得的FeSO4•7H2O需密闭保存,原因是FeSO4有还原性,易被氧化(或FeSO4•7H2O失去结晶水).
⑥上述1000L废水经处理,可获得 FeSO4•7H2O的物质的量是12mol.
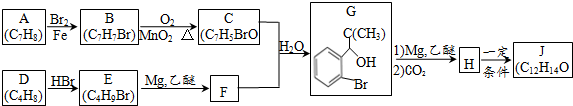

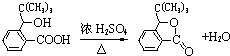 (写明反应条件).
(写明反应条件).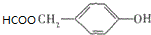 .
. 的路线流程图(其它试剂任选).(合成路线流程图表达方法例如下
的路线流程图(其它试剂任选).(合成路线流程图表达方法例如下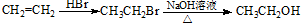 :)
:)