13.从图中表示的各物质能量变化推断下列热化学方程式正确的是(a、b均为正数)( )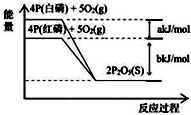

| A. | 4P(白磷)+5O2(g)═2P2O5(S);△H1=+(a+b)kJ/mol | |
| B. | 4P(红磷)+5O2(g)═2P2O5(S);△H2=-(b)kJ/mol | |
| C. | 4P+5O2═2P2O5(s);△H3=+(a+b)kJ/mol | |
| D. | P(白磷)═P(红磷);△H4=+(a)kJ/mol |
12.已知反应:①101kPa时,2C(s)+O 2(g)═2CO(g)△H=-221kJ•mol-1②稀溶液中,
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1下列结论正确的是( )
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1下列结论正确的是( )
| A. | 碳的燃烧热大于110.5 kJ•mol-1 | |
| B. | ①的反应热为221 kJ•mol-1 | |
| C. | 浓硫酸与稀NaOH溶液反应的成1 mol水,放出57.3 kJ热量 | |
| D. | 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
11.根据热化学方程式(在101kPa时):S(s)+O2(g)=SO2(g)△H=-297.23kJ/mol 分析下列说法中不正确的是( )
| A. | S的燃烧热为 297.2 kJ/mol | |
| B. | S(g)+O2(g)=SO2(g)放出的热量大于297.2 kJ | |
| C. | S(g)+O2(g)=SO2(g)放出的热量小于297.2 kJ | |
| D. | 形成1 mol SO 2中的化学键所释放的总能量大于断裂1 mol S(s)和1 mol O2(g)中的化学键所吸收的总能量 |
10.下列物质在常温下发生水解时,对应的水解方程式正确的是( )
| A. | Na2CO3:CO32-+H2O?2OH-+CO2↑ | B. | NH4NO3:NH4++H2O?NH3•H2O+H+ | ||
| C. | CuSO4:Cu2++2H2O?Cu(OH)2↓+2H+ | D. | KF:F-+H2O═HF+OH- |
9.下面关于水解应用的说法错误的是( )
| A. | 用热水溶解纯碱能够提高去油污的效果 | |
| B. | 配制氯化铁溶液时滴加几滴稀盐酸可以防止氢氧化铁形成 | |
| C. | 硫酸铵和草木灰混合施用到农田可以增强肥效 | |
| D. | 盐碱地(含NaCl、Na2CO3)施加适量石膏可以降低土壤的碱性 |
8.下列有关物质的性质及应用说法正确的是( )
| A. | 干燥的Cl2和氯水均能使鲜花褪色 | |
| B. | SiO2具有导电性,可用于制造半导体材料 | |
| C. | 某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ | |
| D. | Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性后者表现出漂白性 |
5.Fe和Mg与H2SO4反应的实验如下:
关于上述实验说法不合理的是( )
实验 | 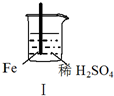 | 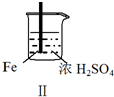 | 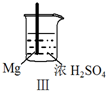 | 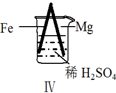 |
现象 | Fe表面产生大量无色气泡 | Fe表面产生气泡后迅速停止 | Mg表面迅速产生大量气泡 | Fe表面有大量气泡,Mg表面有少量气泡 |
| A. | I中产生气体的原因是:Fe+2H+═Fe2++H2↑ | |
| B. | 取出Ⅱ中的铁棒放入CuSO4溶液立即析出亮红色固体 | |
| C. | Ⅲ中现象说明Mg在浓H2SO4中没被钝化 | |
| D. | Ⅳ中现象说明Mg的金属性比Fe强 |
4.有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶液,只有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成;
⑥A与E的溶液中具有相同的阳离子.根据上述实验填空:
(1)写出B、D的化学式:BKCl,DCuSO4;
(2)A受热分解的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)将含0.01mol A的溶液与含0.02mol E的溶液反应后,向溶液中滴加0.1mol•L-1稀盐酸.
下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是C;
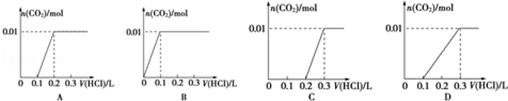
(4)向C中滴加过量E溶液,可用一个离子方程式表示Al3++4OH-=AlO2-+H2O;若在1L 0.1mol/L C溶液中加入175mL 2mol/L的E溶液,生成沉淀的物质的量是0.05mol.
0 152732 152740 152746 152750 152756 152758 152762 152768 152770 152776 152782 152786 152788 152792 152798 152800 152806 152810 152812 152816 152818 152822 152824 152826 152827 152828 152830 152831 152832 152834 152836 152840 152842 152846 152848 152852 152858 152860 152866 152870 152872 152876 152882 152888 152890 152896 152900 152902 152908 152912 152918 152926 203614
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3-OH- Cl- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶液,只有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成;
⑥A与E的溶液中具有相同的阳离子.根据上述实验填空:
(1)写出B、D的化学式:BKCl,DCuSO4;
(2)A受热分解的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)将含0.01mol A的溶液与含0.02mol E的溶液反应后,向溶液中滴加0.1mol•L-1稀盐酸.
下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是C;

(4)向C中滴加过量E溶液,可用一个离子方程式表示Al3++4OH-=AlO2-+H2O;若在1L 0.1mol/L C溶液中加入175mL 2mol/L的E溶液,生成沉淀的物质的量是0.05mol.
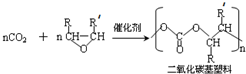 (-R、-R′代表烃基或氢原子)
(-R、-R′代表烃基或氢原子)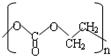 的单体是CO2和
的单体是CO2和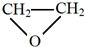 .
.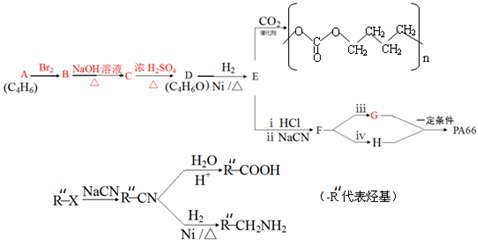
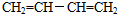 ,名称是1,3-丁二烯.
,名称是1,3-丁二烯.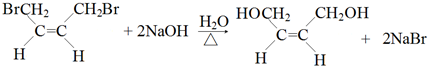 .
.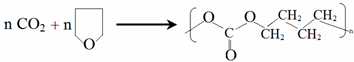 .
.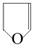 .
.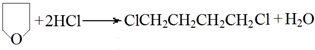 .
.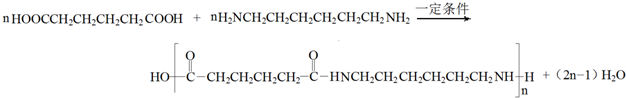 .
.