19.下列各组中的两种物质相互反应时,无论哪种过量,都可以用同一个离子方程式表示的组数是( )
①亚硫酸钠溶液与稀盐酸 ②偏铝酸钠溶液与盐酸 ③二氧化碳与氢氧化钠溶液
④氯化铝与氨水 ⑤碳酸氢钠溶液与澄清石灰水
⑥碳酸氢钙溶液与澄清石灰水 ⑦苯酚钠溶液中通入二氧化碳.
①亚硫酸钠溶液与稀盐酸 ②偏铝酸钠溶液与盐酸 ③二氧化碳与氢氧化钠溶液
④氯化铝与氨水 ⑤碳酸氢钠溶液与澄清石灰水
⑥碳酸氢钙溶液与澄清石灰水 ⑦苯酚钠溶液中通入二氧化碳.
| A. | 2组 | B. | 3组 | C. | 4组 | D. | 5组 |
18.下列关于如图所示转化关系(X代表卤素)的说法错误的是( )
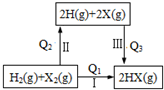

| A. | Q3>0 | B. | Q1=Q2+Q3 | ||
| C. | 按Cl、Br、I的顺序,Q2依次增大 | D. | Q1越大,HX越稳定 |
17. 在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列说法正确的是( )
在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列说法正确的是( )
 在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列说法正确的是( )
在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,下列说法正确的是( )| A. | 外电路的电流方向为:X→外电路→Y | |
| B. | X极上发生的是还原反应 | |
| C. | 溶液中氢离子向X极移动 | |
| D. | 若两电极都是金属,则它们的活动性顺序为X>Y |
16.下列有关化学基本概念的判断依据正确的是( )
| A. | 弱电解质:溶液的导电能力弱 | B. | 共价化合物:含有共价键 | ||
| C. | 离子化合物:含有离子键 | D. | 金属晶体:能够导电 |
15.金属能导电的原因是( )
| A. | 金属阳离子与自由电子间的作用较弱 | |
| B. | 金属在外加电场作用下可失去电子 | |
| C. | 金属阳离子在外加电场作用下可发生定向移动 | |
| D. | 自由电子在外加电场作用下可发生定向移动 |
14.能导电的电解质是( )
| A. | 氯化钠溶液 | B. | 金属铜 | C. | 熔融硝酸钾 | D. | 酒精 |
13.化学与社会、生活密切相关.下列有关说法错误的是( )
| A. | 地球上99%以上的溴蕴藏在海洋中 | |
| B. | 用食醋可除去热水壶内壁的水垢 | |
| C. | 在水库铁闸门上接装铜块可减缓铁闸门腐蚀 | |
| D. | 将煤气化或液化可减少污染、提高燃烧效率 |
10.草酸钴用途广泛,可用于指示剂和催化剂制备.一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4•2H2O工艺流程如图1:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中加入Na2SO3的目的是将Fe3+、Co3+还原(填离子符号)以便固体溶解.该步反应的离子方程式为SO32-+2Fe3++H2O═SO42-+2Fe2++2H+或SO32-+2Co3++H2O═SO42-+2Co2++2H+(写一个).
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价.该反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O.
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是R3++3H2O?R(OH)3+3H+,加入碳酸钠后,H+与CO32-反应,使水解平衡右移,从而产生沉淀.
(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去溶液中的Mn2+;使用萃取剂适宜的pH=B(填序号)左右:
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c (Ca2+)=0.7.
0 152711 152719 152725 152729 152735 152737 152741 152747 152749 152755 152761 152765 152767 152771 152777 152779 152785 152789 152791 152795 152797 152801 152803 152805 152806 152807 152809 152810 152811 152813 152815 152819 152821 152825 152827 152831 152837 152839 152845 152849 152851 152855 152861 152867 152869 152875 152879 152881 152887 152891 152897 152905 203614

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,氯元素被还原为最低价.该反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O.
(3)利用平衡移动原理分析:加Na2CO3能使浸出液中Fe3+、Al3+转化成氢氧化物沉淀的原因是R3++3H2O?R(OH)3+3H+,加入碳酸钠后,H+与CO32-反应,使水解平衡右移,从而产生沉淀.
(4)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去溶液中的Mn2+;使用萃取剂适宜的pH=B(填序号)左右:
A.2.0 B.3.0 C. 4.0
(5)滤液Ⅰ“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c (Ca2+)=0.7.

 .
. .
. .
. )的合成线路:
)的合成线路: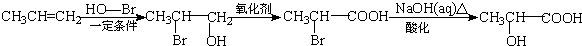 .
.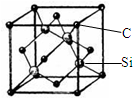 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答:
铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.请回答: