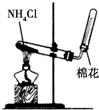
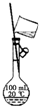
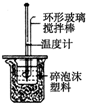
10.维生素C具有的性质是( )
| A. | 难溶于水 | B. | 易溶于水 | C. | 弱还原性 | D. | 强氧化性 |
9.下列气体属于无色、无味、有毒的气体是( )
| A. | CO | B. | SO2 | C. | CO2 | D. | H2S |
8.我国卫生部门制定的《关于宣传吸烟有毒与控制吸烟》的通知中规定:“中学生不准吸烟”.香烟燃烧产生的烟气中,有多种有害物质,其中尼古丁(C10H14N2)对人体危害最大,下列说法正确的是( )
| A. | 尼古丁是由26个原子构成的物质 | |
| B. | 尼古丁中C、H、N 三种元素的质量比为:10:14:2 | |
| C. | 尼古丁的相对分子质量是162g | |
| D. | 尼古丁中氮元素的质量分数为17.3% |
7.目前野生动植物濒临灭绝的主要原因( )
| A. | 水土流失 | B. | 森林的破坏 | C. | 自然灾害 | D. | 气候变暖 |
6.下列关于食品添加剂的叙述中不正确的是( )
| A. | 醋可同时用作防腐剂和调味剂 | |
| B. | 亚硝酸钠可以用作防腐剂,但不宜过量 | |
| C. | 我国应禁止使用味精 | |
| D. | 绝大多数食品添加剂在过量使用时对人体有害的 |
5.欲将蛋白质从水中析出而又不改变它的性质应加入( )
| A. | 甲醛溶液 | B. | 饱和Na2SO4溶液 | C. | CuSO4溶液 | D. | 浓硫酸 |
4.下列物质碱性最强的是( )
| A. | LiOH | B. | KOH | C. | RbOH | D. | NaOH |
2.卤素单质的性质活泼,卤素的化合物应用广泛,运用化学反应原理研究卤族元素的有关性质具有重要意义.
(1)下列关于氯水的叙述正确的是AEF(填写序号).
A.氯水中存在两种电离平衡
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25℃时有关弱酸的电离平衡常数:
写出84消毒液(主要成分为NaClO)露置在空气中发生反应的有关化学方程式NaClO+CO2+H2O═HClO+NaHCO3.若将84消毒液与洁厕剂(含有浓盐酸)混合使用可能会导致中毒,请用离子方程式解释有关原因ClO-+Cl-+2H+═Cl2↑+H2O.
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.工业上制备ClO2的反应原理常采用:2NaClO3+4HCl(浓)═2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是B(填序号).
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ClO2,则转移电子的物质的量为0.1mol.
③ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.现用ClO2将CN-氧化,有两种气体生成,其离子反应方程式为2ClO2+2CN-=N2↑+2CO2↑+2Cl-.
0 152681 152689 152695 152699 152705 152707 152711 152717 152719 152725 152731 152735 152737 152741 152747 152749 152755 152759 152761 152765 152767 152771 152773 152775 152776 152777 152779 152780 152781 152783 152785 152789 152791 152795 152797 152801 152807 152809 152815 152819 152821 152825 152831 152837 152839 152845 152849 152851 152857 152861 152867 152875 203614
(1)下列关于氯水的叙述正确的是AEF(填写序号).
A.氯水中存在两种电离平衡
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=3.0×10-8 | K1=4.4×10-7,K2=4.7×10-11 |
(3)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.工业上制备ClO2的反应原理常采用:2NaClO3+4HCl(浓)═2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是B(填序号).
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ClO2,则转移电子的物质的量为0.1mol.
③ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.现用ClO2将CN-氧化,有两种气体生成,其离子反应方程式为2ClO2+2CN-=N2↑+2CO2↑+2Cl-.
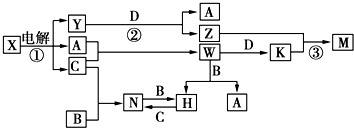
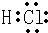 .
.