10.常温下,下列溶液中各微粒的物质的量浓度关系正确的是( )
| A. | 浓度为0.1 mol/L CH3COOH与0.1 mol/L CH3COONa混合后溶液呈弱酸性,则c(CH3COOH>c(Na+)>c(CH3COO-) | |
| B. | 相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸三种溶液中由水电离出的c(H+):①>②>③ | |
| C. | NaHCO3溶液:c(OH-)-c(H+)=c((HCO3-)+2c(H2CO3) | |
| D. | 等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
9.25℃时,某溶液中水电离的OH-浓度为1×10-5,该溶液可能是( )
| A. | NaOH | B. | HCl | C. | NaCl | D. | Na2CO3 |
5.下表列出了①~⑨九种元素在周期表中的位置.
请按要求回答下列问题.
(1)这九种元素中,原子半径最大的是(填元素符号)K;元素⑤的原子结构示意图为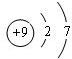 .
.
(2)③、④、⑤三种元素的气态氢化物中,热稳定性最弱的物质是(填化学式)CH4.
(3)写出元素⑧的单质与水反应的化学方程式:2K+2H2O═2KOH+H2↑.
(4)写出元素⑦的单质与元素⑨的钠盐溶液反应的离子方程式:Cl2+2Br-═Br2+2Cl-.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ||||||
| 4 | ⑧ | ⑨ | ||||||
(1)这九种元素中,原子半径最大的是(填元素符号)K;元素⑤的原子结构示意图为
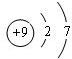 .
.(2)③、④、⑤三种元素的气态氢化物中,热稳定性最弱的物质是(填化学式)CH4.
(3)写出元素⑧的单质与水反应的化学方程式:2K+2H2O═2KOH+H2↑.
(4)写出元素⑦的单质与元素⑨的钠盐溶液反应的离子方程式:Cl2+2Br-═Br2+2Cl-.
4.某烃的结构简式为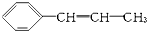 ,它可能具有的性质是( )
,它可能具有的性质是( )
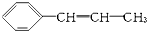 ,它可能具有的性质是( )
,它可能具有的性质是( )| A. | 易溶于水,也易溶于有机溶剂 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色 | |
| C. | 能发生聚合反应,其产物可表示为 | |
| D. | 能使溴水褪色,但不能使酸性KMnO4溶液褪色 |
3.下列关于石油的说法正确的是( )
| A. | 石油裂解的目的主要是为了把重油分解成相对分子量较小的烃 | |
| B. | 石油裂解可以得到氯乙烯 | |
| C. | 石油分馏能得到不同沸点范围的产物 | |
| D. | 石油裂化是物理变化 |
2.将100mL 4mol/L Cu(NO3)2溶液电解一段时间(用碳电极),在阳极收集到1.12L气体.将电解后溶液中加入铁粉,最多溶解的铁粉质量为(设反应前后溶液体积不变)( )
| A. | 16.8g | B. | 22.4g | C. | 21g | D. | 19.6g |
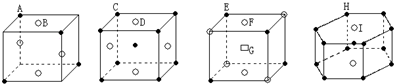
1.下列晶胞所对应的化学式正确的是( )
0 152679 152687 152693 152697 152703 152705 152709 152715 152717 152723 152729 152733 152735 152739 152745 152747 152753 152757 152759 152763 152765 152769 152771 152773 152774 152775 152777 152778 152779 152781 152783 152787 152789 152793 152795 152799 152805 152807 152813 152817 152819 152823 152829 152835 152837 152843 152847 152849 152855 152859 152865 152873 203614

| A. | A3B4 | B. | CD | C. | EF3G2 | D. | H5I |

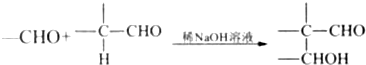
 .
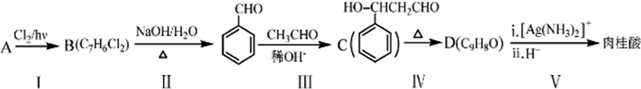
. .肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是
.肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是 .
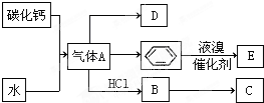
.
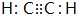 ;D的空间构型为平面结构,键角为120°;
;D的空间构型为平面结构,键角为120°; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应.
+HBr,其反应类型为取代反应.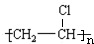 ,其反应类型为加聚反应.
,其反应类型为加聚反应.