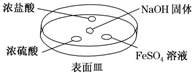
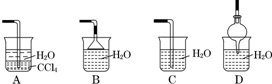
13.在恒容的密闭容器中,一定温度下可逆反应A(g)+3B(g)?2C(g)达到化学反应平衡的标志是( )
| A. | 单位时间内消耗n molA,同时消耗3n mol B | |
| B. | A、B、C三者的浓度相同 | |
| C. | 容器内气体的压强不随时间的变化而变化 | |
| D. | 混合气体的密度不在发生变化 |
12.如图所示,a、b是多孔石墨电极,某同学按图示装置进行如下实验:断开K2,闭合K1一段时间,观察到两只玻璃管内都有气泡将电极包围,此时断开K1,闭合K2,观察到电流计A的指针有偏转.下列说法正确的是( )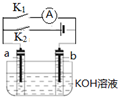

| A. | 断开K2,闭合K1一段时间,溶液的pH要变大 | |
| B. | 断开K1,闭合K2时,b极上的电极反应式为 2H++2e-═H2↑ | |
| C. | 断开K1,闭合K2时,OH-向b极移动 | |
| D. | 断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-═O2↑+2H2O |
11.钢铁发生吸氧腐蚀时,负极上发生的电极反应是( )
| A. | 2H++2e-═H2 | B. | Fe-2e-═Fe2+ | ||
| C. | 2H2O+O2+4e-═4OH- | D. | Fe+2e-═Fe2+ |
9.下列离子方程式中不正确的是( )
| A. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 硫代硫酸钠与稀硫酸反应的离子方程式为S2O32-+2H+═SO42-+S↓+H2O | |
| C. | 利用水解原理制备纳米材料TiCl4+(2+n)H2O?4HCl+TiO2?nH2O↓ | |
| D. | 向明矾溶液中滴加Ba(OH)2至SO42-恰好完全沉淀时Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
7.软锰矿(主要成分为MnO2)可用于制备锰及其化合物.
(1)早期冶炼金属锰的一种方法是先煅烧软锰矿生成Mn3O4,再利用铝热反应原理制得锰,该铝热反应的化学方程式为8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn.
(2)现代冶炼金属锰的一种工艺流程如下图所示:
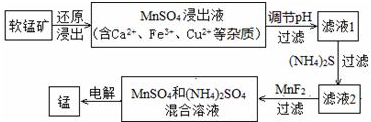
下表为t℃时,有关物质的pKsp(注:pKsp=-lgKsp).
软锰矿还原浸出的反应为:
12MnO2+C6H12O6+12H2SO4=12MnSO4+CO2↑+18H2O
①该反应中,还原剂为C6H12O6.写出一种能提高还原浸出速率的措施:升高反应温度或将软锰矿研细等.
②滤液1的pH>(填“>”、“<”或“=”)MnSO4浸出液的pH.
③加入MnF2的主要目的是除去Ca2+(填Ca2+、Fe3+或Cu2+)
(3)由MnSO4制取MnCO3
往MnSO4溶液中加入过量NH4HCO3溶液,该反应的离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;若往MnSO4溶液中加入(NH4)2CO3溶液,还会产生Mn(OH)2,可能的原因有:MnCO3(s)+2OH-(aq)?Mn(OH)2(s)+CO32-(aq),t℃时,计算该反应的平衡常数K=100(填数值).
(1)早期冶炼金属锰的一种方法是先煅烧软锰矿生成Mn3O4,再利用铝热反应原理制得锰,该铝热反应的化学方程式为8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn.
(2)现代冶炼金属锰的一种工艺流程如下图所示:

下表为t℃时,有关物质的pKsp(注:pKsp=-lgKsp).
| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
12MnO2+C6H12O6+12H2SO4=12MnSO4+CO2↑+18H2O
①该反应中,还原剂为C6H12O6.写出一种能提高还原浸出速率的措施:升高反应温度或将软锰矿研细等.
②滤液1的pH>(填“>”、“<”或“=”)MnSO4浸出液的pH.
③加入MnF2的主要目的是除去Ca2+(填Ca2+、Fe3+或Cu2+)
(3)由MnSO4制取MnCO3
往MnSO4溶液中加入过量NH4HCO3溶液,该反应的离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;若往MnSO4溶液中加入(NH4)2CO3溶液,还会产生Mn(OH)2,可能的原因有:MnCO3(s)+2OH-(aq)?Mn(OH)2(s)+CO32-(aq),t℃时,计算该反应的平衡常数K=100(填数值).
5.下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A. | pH相同的①CH3COONa②NaHCO3③NaAlO2三份溶液中的c(Na+):②>③>① | |
| B. | 将0.5 mol/L的Na2CO3溶液与amol/L的NaHCO3溶液等体积混合,c(Na+)<c(CO32-)+c(HCO3-)+c(H2CO3) | |
| C. | 10mL0.1mol/LCH3COOH溶液与20mL0.1mol/LNaOH溶液混合后,溶液中离子浓度关系:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) | |
| D. | 25℃某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-dmol/L |
4.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
0 152658 152666 152672 152676 152682 152684 152688 152694 152696 152702 152708 152712 152714 152718 152724 152726 152732 152736 152738 152742 152744 152748 152750 152752 152753 152754 152756 152757 152758 152760 152762 152766 152768 152772 152774 152778 152784 152786 152792 152796 152798 152802 152808 152814 152816 152822 152826 152828 152834 152838 152844 152852 203614
| A. | 标准状况下,33.6LHF中含有氟原子的数目为1.5NA | |
| B. | 17g-OH中电子数为9NA | |
| C. | 氢氧燃料电池正极消耗22.4 L气体时,电路中通过的电子数目为2NA | |
| D. | 标准状况下,0.1mol Cl2溶于水,转移电子数为0.1NA |
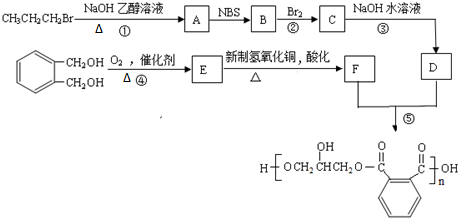
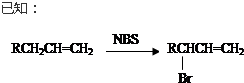
 .
. .
.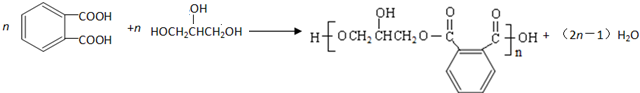 .
. .
.