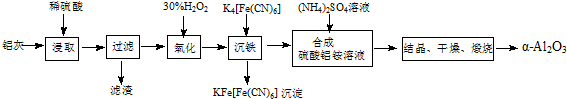
3.由锌、铁、铝、镁四种金属中的两种组成的混合物11.5克,与足量的盐酸反应产生的氢气标准状况下为11.2升,则两种金属组成的混合物是( )
| A. | 锌与镁 | B. | 铁与锌 | C. | 铝与铁 | D. | 镁与铁 |
2.只用一种试剂可以区别NH4Cl、MgCl2、FeSO4、AlCl3、FeCl3五种溶液,这种试剂是( )
| A. | 稀硫酸 | B. | 氨水 | C. | AgNO3 溶液 | D. | NaOH溶液 |
1.化学与环境、科学、技术密切相关.下列有关说法中正确的是( )
| A. | 可使用填埋法处理未经分类的生活垃圾 | |
| B. | 光化学烟雾的形成与汽车尾气中的氮氧化物有关 | |
| C. | 光导纤维都是有机高分子化合物 | |
| D. | “鸟巢”使用钒氮合金钢,该合金熔点、硬度和强度均比纯铁高 |
20.下列对某些问题的认识正确的是( )
| A. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| B. | Na的金属性比Cu强,故可用Na与CuSO4溶液反应制取Cu | |
| C. | 不能用带玻璃塞的玻璃瓶盛放碱液 | |
| D. | 玻璃、水泥、陶瓷、水晶都是重要的硅酸盐材料 |
19.向A、B、C和D四支试管中的溶液分别进行表中的操作,通过观察到的实验现象得出的结论正确的是
( )
| 操作 | 现象 | 结论 | |
| A | ①滴加稀HNO3 ②滴加BaCl2溶液 | 无明显现象 白色沉淀 | 原溶液一定含Ag+ |
| B | 滴加稀盐酸 | 有大量气泡产生 | 原溶液一定含CO32- |
| C | ①滴加稀HCl ②滴加AgNO3溶液 | 无明显现象 白色沉淀 | 原溶液一定含Cl- |
| D | ①加KSCN溶液 ②滴加氯水 | 无明显现象 溶液呈红色 | 原溶液一定含Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
18. (1)CO2分子的电子式为
(1)CO2分子的电子式为 ;Na2O2的电子式为
;Na2O2的电子式为
(2)能使0.1mol/L乙酸溶液的电离程度以及pH都增大的是ad.(选填序号)
a.加水稀释 b.加入少量乙酸钠固体 c.通氯化氢 d.加入少量苛性钠固体
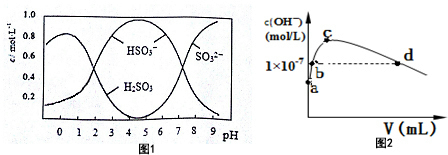
(3)葡萄酒中常用Na2S2O5做抗氧化剂.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图1所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol•L-1],此时溶液中c(SO32-)≤0.05mol•L-1.
(5)请写出用NaOH溶液完全吸收含等物质的量的NO、NO2混合气体的离子方程式NO+NO2+2OH-=2NO2-+H2O.
(6)常温下,向1L pH=10的 NaOH溶液中持续通入CO2.通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图2所示
①c点溶液中离子浓度由大至小的关系是:c(Na+)>c(CO32-)>c(HCO3-).
②a点溶液中由水电离产生的c(H+)=1×10-10mol/L;b点溶液中c(H+)小于1×10-7mol/L(填写“等于”、“大于”或“小于”).
(7)部分弱酸的电离平衡常数如下表:
下列选项错误的有bc.
a.2HCOOH+CO32-═2HCOO-+H2O+CO2↑
b.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者
c.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者.
 (1)CO2分子的电子式为
(1)CO2分子的电子式为 ;Na2O2的电子式为
;Na2O2的电子式为
(2)能使0.1mol/L乙酸溶液的电离程度以及pH都增大的是ad.(选填序号)
a.加水稀释 b.加入少量乙酸钠固体 c.通氯化氢 d.加入少量苛性钠固体
(3)葡萄酒中常用Na2S2O5做抗氧化剂.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图1所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp[BaSO4]=1×10-10,Ksp[BaSO3]=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全[c(SO42-)≤1×10-5mol•L-1],此时溶液中c(SO32-)≤0.05mol•L-1.
(5)请写出用NaOH溶液完全吸收含等物质的量的NO、NO2混合气体的离子方程式NO+NO2+2OH-=2NO2-+H2O.
(6)常温下,向1L pH=10的 NaOH溶液中持续通入CO2.通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图2所示
①c点溶液中离子浓度由大至小的关系是:c(Na+)>c(CO32-)>c(HCO3-).
②a点溶液中由水电离产生的c(H+)=1×10-10mol/L;b点溶液中c(H+)小于1×10-7mol/L(填写“等于”、“大于”或“小于”).
(7)部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25°C)) | Ki=1.77×10-14 | Ki=4.9×10-14 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
a.2HCOOH+CO32-═2HCOO-+H2O+CO2↑
b.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者
c.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者.
16.在相同温度下等体积、等物质的量浓度的4种稀溶液:①Na2SO4 ②H2SO3 ③NaHSO3④Na2S,所含带电微粒的数目由多到少的顺序是( )
| A. | ①=④>③=② | B. | ①=④>③>② | C. | ①>④>③>② | D. | ④>①>③>② |
15.研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )
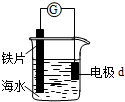

| A. | d为石墨,电流从d流入导线进入铁片 | |
| B. | d为铜片,铜片上电极反应为:O2+2H2O+4e-═4OH- | |
| C. | d为锌块,铁片不易被腐蚀 | |
| D. | d为镁片,铁片上电极反应为:2H++2e-═H2↑ |
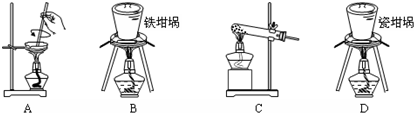
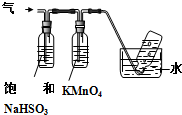
14.下列实验原理或操作,正确的是( )
0 152653 152661 152667 152671 152677 152679 152683 152689 152691 152697 152703 152707 152709 152713 152719 152721 152727 152731 152733 152737 152739 152743 152745 152747 152748 152749 152751 152752 152753 152755 152757 152761 152763 152767 152769 152773 152779 152781 152787 152791 152793 152797 152803 152809 152811 152817 152821 152823 152829 152833 152839 152847 203614
| A. | 用广泛pH试纸测得 0.1mol/L NH4Cl溶液的pH=5.2 | |
| B. | 酸碱中和滴定时锥形瓶用蒸馏水洗涤后,再用待测液润洗后装液进行滴定 | |
| C. | 将碘水倒入分液漏斗,加入适量苯振荡后静置,从分液漏斗下口放出碘的苯溶液 | |
| D. | 常温常压下,将15g NO和8g O2混合,所得混合气体分子总数小于0.5NA |