18.25℃时,电离平衡常数:
回答下列问题:
(1)pH=11的下列四种水溶液:
a.Na2CO3,b.NaClO,c.NaHCO3,d.CH3COONa.溶质的物质的量浓度由大到小的顺序是d>c>b>a(填编号);将NaHCO3溶液蒸干灼烧所得固体名称为碳酸钠.
(2)25℃,0.1mol•L-1的CH3COONa溶液加水稀释过程中,水解平衡将正向移动(填“正向”或“逆向”),其溶液中c(H+)•c(OH-)将不变(填“变大”“变小”或“不变”,下同);$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$将
变大;水解常数其Kb的值是$\frac{1{0}^{-9}}{1.8}$(列出数学表达式并化简).
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1:4.3×10-7 K2:5.6×10-11 | 3.2×10-8 |
(1)pH=11的下列四种水溶液:
a.Na2CO3,b.NaClO,c.NaHCO3,d.CH3COONa.溶质的物质的量浓度由大到小的顺序是d>c>b>a(填编号);将NaHCO3溶液蒸干灼烧所得固体名称为碳酸钠.
(2)25℃,0.1mol•L-1的CH3COONa溶液加水稀释过程中,水解平衡将正向移动(填“正向”或“逆向”),其溶液中c(H+)•c(OH-)将不变(填“变大”“变小”或“不变”,下同);$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$将
变大;水解常数其Kb的值是$\frac{1{0}^{-9}}{1.8}$(列出数学表达式并化简).
17.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | 新制氯水中加入少量固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+cOH-) | |
| B. | pH=9的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1mol•L-1CH3COOH溶液与0.05mol•L-1NaOH溶液等体积混合:2c(H+)+c((CH3COOH)=c(CH3COO-)+2c(OH-) |
16.25℃时,纯水中水电离出的c(H+)=a1,pH=3的盐酸溶液中水电离出的c(H+)=a2,pH=11的氨水溶液中水电离出的c(H+)=a3.将上述盐酸与氨水溶液等体积混合所得溶液中水电离出的c(H+)=a4.下列关系式正确的( )
| A. | a2<a3<a1<a4 | B. | a3=a2<a1<a4 | C. | a2=a3<a4<a1 | D. | a1<a2<a3<a4 |
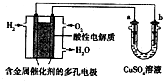
15.用酸性氢氧燃料电池为电源进行电解的实验装置如图所示.下列说法中正确的是( )
0 152636 152644 152650 152654 152660 152662 152666 152672 152674 152680 152686 152690 152692 152696 152702 152704 152710 152714 152716 152720 152722 152726 152728 152730 152731 152732 152734 152735 152736 152738 152740 152744 152746 152750 152752 152756 152762 152764 152770 152774 152776 152780 152786 152792 152794 152800 152804 152806 152812 152816 152822 152830 203614

| A. | 燃料电池工作时,正极反应为:O2+4H++4e-═2H2O | |
| B. | a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 | |
| C. | a极是纯铜,b极是粗铜时,可以达到铜的精炼目的 | |
| D. | a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
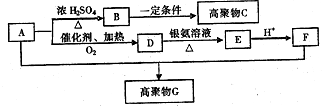 有机物A常用作有机合成的中间体.15.2g该有机物燃烧生成26.4gCO2和14.4gH2O;质谱图表明其相对分子质量为76,红外光谱分析表明A分子中含有O-H键和C-O键.核磁共振氢谱上有三个峰,峰面积之比为2:1:1.A能发生如图转化:
有机物A常用作有机合成的中间体.15.2g该有机物燃烧生成26.4gCO2和14.4gH2O;质谱图表明其相对分子质量为76,红外光谱分析表明A分子中含有O-H键和C-O键.核磁共振氢谱上有三个峰,峰面积之比为2:1:1.A能发生如图转化: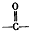 ,则H的结构简式可能为CH3CH2CHO、
,则H的结构简式可能为CH3CH2CHO、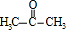 .
.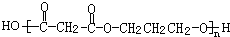 +(2n-1)H2O.
+(2n-1)H2O.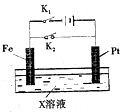 如图是一个电化学过程的示意图,请回答下列问题:
如图是一个电化学过程的示意图,请回答下列问题: