4.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 78g由Na2S和Na2O2组成的固体混合物,含有的阴离子数为NA | |
| B. | 标准状况下,22.4L CCl4中含有的分子数为NA | |
| C. | 将1mol FeCl3水解制成胶体,所得胶体中含有的胶体粒子数NA | |
| D. | 2.0gH218O与D2O的混合物中所含中子数为NA |
3.某化学活动小组按下图所示流程由粗氧化铜样品(含少量氧化亚铁及不溶于酸的杂质)制取无水硫酸铜.
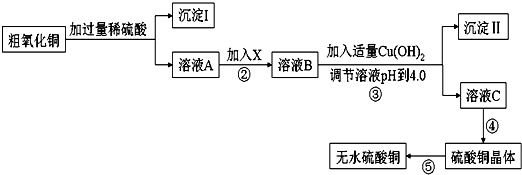
已知Fe3+、Cu2+、Fe2+三种离子在水溶液中形成氢氧化物沉淀的pH范围如下图所示:
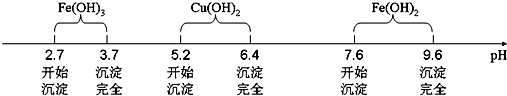
请回答下列问题:
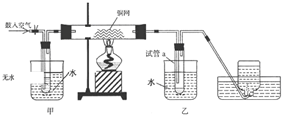
(1)在整个实验过程中,下列实验装置不可能用到的是①③(填序号)
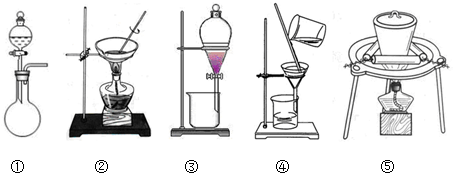
(2)溶液A中所含溶质为CuSO4、FeSO4、H2SO4;
(3)物质X应选用②(填序号),沉淀Ⅱ的主要成分是Fe(OH)3
①氯水 ②双氧水 ③铁粉 ④高锰酸钾
(4)从溶液C中制取硫酸铜晶体的实验操作为蒸发浓缩、冷却结晶、过滤、自然干燥.
(5)用“间接碘量法”可以测定溶液A中Cu2+(不含能与I-发生反应的杂质)的浓度.过程如下:
第一步:移取10.00mL溶液A于100mL容量瓶,加水定容至100mL.
第二步:取稀释后试液20.00mL于锥形瓶中,加入过量KI固体,充分反应生成白色沉淀与碘单质.
第三步:以淀粉溶液为指示剂,用0.05000mol•L-1的Na2S2O3标准溶液滴定,前后共测定三组.达到滴定终点时,消耗Na2S2O3标准溶液的体积如下表:
(已知:I2+2S2O32-═2I-+S4O62-)
①CuSO4溶液与KI的反应的离子方程式为2Cu2++4I-═2CuI↓+I2.
②滴定中,试液Na2S2O3应放在碱式滴定管(填“酸式滴定管”或“碱式滴定管”),判断滴定终点的依据是最后一滴试液滴入,溶液由蓝色变为无色,振荡半分钟,溶液无明显变化.
③溶液A中c(Cu2+)=0.5000mol•L-1.

已知Fe3+、Cu2+、Fe2+三种离子在水溶液中形成氢氧化物沉淀的pH范围如下图所示:

请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是①③(填序号)

(2)溶液A中所含溶质为CuSO4、FeSO4、H2SO4;
(3)物质X应选用②(填序号),沉淀Ⅱ的主要成分是Fe(OH)3
①氯水 ②双氧水 ③铁粉 ④高锰酸钾
(4)从溶液C中制取硫酸铜晶体的实验操作为蒸发浓缩、冷却结晶、过滤、自然干燥.
(5)用“间接碘量法”可以测定溶液A中Cu2+(不含能与I-发生反应的杂质)的浓度.过程如下:
第一步:移取10.00mL溶液A于100mL容量瓶,加水定容至100mL.
第二步:取稀释后试液20.00mL于锥形瓶中,加入过量KI固体,充分反应生成白色沉淀与碘单质.
第三步:以淀粉溶液为指示剂,用0.05000mol•L-1的Na2S2O3标准溶液滴定,前后共测定三组.达到滴定终点时,消耗Na2S2O3标准溶液的体积如下表:
(已知:I2+2S2O32-═2I-+S4O62-)
| 滴定次数 | 第一次 | 第二次 | 第三次 |
| 滴定前读数(mL) | 0.10 | 0.36 | 1.10 |
| 滴定滴定后读数(mL) | 20.12 | 20.34 | 22.12 |
②滴定中,试液Na2S2O3应放在碱式滴定管(填“酸式滴定管”或“碱式滴定管”),判断滴定终点的依据是最后一滴试液滴入,溶液由蓝色变为无色,振荡半分钟,溶液无明显变化.
③溶液A中c(Cu2+)=0.5000mol•L-1.
2.亚氯酸钠是一种高效氧化型漂白剂,主要用于棉纺、亚麻、纸浆等漂白.亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2是毒性很大的气体.经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).在25℃时,下列分析正确的是( )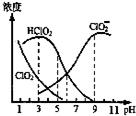

| A. | 使用该漂白剂的最佳pH为3 | |
| B. | pH=5时,溶液中$\frac{c(Cl{{O}_{2}}^{-})}{c(HCl{O}_{2})}$═$\frac{1}{10}$ | |
| C. | pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c( ClO2-)>c( ClO2)>c( Cl-) | |
| D. | NaClO2溶液加水稀释所有离子浓度均减小 |
20.氢氰酸(HCN)的下列性质中,可以证明它是弱电解质的是( )
| A. | 1 mol•L-1 HCN溶液的pH约为3 | |
| B. | HCN易溶于水 | |
| C. | 10 mL 1 mol•L-1 HCN溶液恰好与10 mL 1 mol•L-1NaOH溶液完全反应 | |
| D. | 在相同条件下,HCN溶液的导电性比强酸溶液的弱 |
19.在25℃、1.01×105 Pa下,反应2N2O5(g)═4NO2(g)+O2(g)△H=+56.7kJ•mol-1能自发进行的合理解释是( )
| A. | 该反应是分解反应 | B. | 该反应的熵增效应大于焓变效应 | ||
| C. | 该反应是熵减反应 | D. | 该反应是放热反应 |
17.设NA为阿伏加德罗常数,下列说法正确的是( )
0 152616 152624 152630 152634 152640 152642 152646 152652 152654 152660 152666 152670 152672 152676 152682 152684 152690 152694 152696 152700 152702 152706 152708 152710 152711 152712 152714 152715 152716 152718 152720 152724 152726 152730 152732 152736 152742 152744 152750 152754 152756 152760 152766 152772 152774 152780 152784 152786 152792 152796 152802 152810 203614
| A. | 23 g钠在氧气中完全燃烧失电子数为0.5NA | |
| B. | 标准状况下,22.4 L苯所含的分子数 | |
| C. | 室温下,8 g甲烷含有共价键数为2NA | |
| D. | 1 L 1 mol•L-1硫酸溶液所含的H+数 |
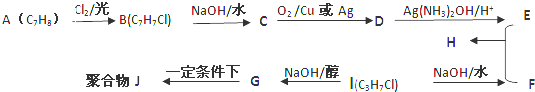
 ,D的官能团名称醛基.
,D的官能团名称醛基. +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. +CH3CH(OH)CH3$→_{△}^{浓硫酸}$
+CH3CH(OH)CH3$→_{△}^{浓硫酸}$ +H2O.
+H2O.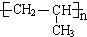 .
.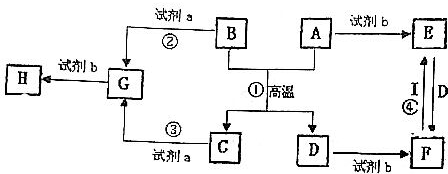
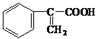 )和甲醇反应制得.
)和甲醇反应制得.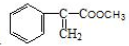
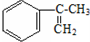 经过四步不同类型的反应制得阿托酸.
经过四步不同类型的反应制得阿托酸.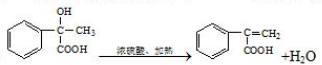 .
.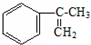 多两个碳原子的一种同系物,且A的所有碳原子可以处于同一平面上.写出A的结构简式
多两个碳原子的一种同系物,且A的所有碳原子可以处于同一平面上.写出A的结构简式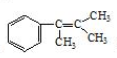 .
.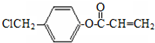 是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为
是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为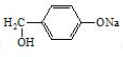 、
、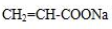 .
.
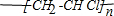
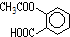 ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为3mol.