12.过氧化钠和水反应的离子方程式是( )
| A. | Na2O2+2H2O═2Na++2OH-+H2↑ | B. | 2O22-+4H+═4OH-+O2↑ | ||
| C. | Na2O2+2H2O═2Na++2OH-+O2↑ | D. | 2Na2O2+2H2O═4Na++4OH-+O2↑ |
11.下列关于硫酸的叙述中,正确的是( )
| A. | 浓硫酸具有吸水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸有氧化性,稀硫酸无氧化性 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 稀释浓硫酸时,应将其沿着器壁慢慢加入到水中,并用玻璃棒不断搅拌 |
9.下列技术应用中,其工作原理不涉及化学反应的是( )
| A. |  火炬燃烧 | B. |  风力发电 | C. |  粮食酿醋 | D. |  高炉炼铁 |
8.环保意识是重要的公民意识.下列气体不属于空气质量日报监测指标的是( )
| A. | SO2 | B. | CO | C. | N2 | D. | NO2 |
7.硝酸是氧化性酸,其本质是NO3-有氧化性,某课外实验小组进行了下列有关NO3-氧化性的探究(实验均在通风橱中完成).
(1)实验Ⅰ中,铝片作负(填“正”或“负”)极.液面上方产生红棕色气体的化学方程式是2NO+O2=2NO2.
(2)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是Al开始作电池的负极,Al在浓硝酸中迅速生成致密氧化膜后,Cu作负极.
查阅资料:活泼金属与1mol•L-1稀硝酸反应有H2和NH4+生成,NH4+生成的原理是产生H2的过程中NO3-被还原.
 (3)用如图装置进行实验Ⅲ:溶液X为1mol•L-1稀硝酸溶液,观察到电流计指针向右偏转.
(3)用如图装置进行实验Ⅲ:溶液X为1mol•L-1稀硝酸溶液,观察到电流计指针向右偏转.
①反应后的溶液中含NH4+.实验室检验NH4+的方法是取少量待检溶液于试管中,加入浓NaOH溶液,加热,若产生使湿润的红色石蕊试纸变蓝的气体,则溶液中含NH4+.
②生成NH4+的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
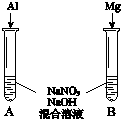
(4)进一步探究碱性条件下NO3-的氧化性,进行实验Ⅳ:
①观察到A中有NH3生成,B中无明显现象.A、B产生不同现象的解释是Al与NaOH溶液反应产生H2的过程中可将NO3-还原为NH3,而Mg不能与NaOH.
②A中生成NH3的离子方程式是8Al+3NO3-+5OH-+2H2O=3NH3↑+8AlO2-.
(5)将铝粉加入到NaNO3溶液中无明显现象,结合实验Ⅲ和Ⅳ说明理由因为铝与中性的硝酸钠溶液无生成H2的过程,NO3-无法被还原.
0 152602 152610 152616 152620 152626 152628 152632 152638 152640 152646 152652 152656 152658 152662 152668 152670 152676 152680 152682 152686 152688 152692 152694 152696 152697 152698 152700 152701 152702 152704 152706 152710 152712 152716 152718 152722 152728 152730 152736 152740 152742 152746 152752 152758 152760 152766 152770 152772 152778 152782 152788 152796 203614
| 实验装置 | 编号 | 溶液X | 实验现象 |
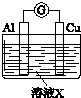 | 实验Ⅰ | 6mol•L-1稀硝酸 | 电流计指针向右偏转,铜片表面产生无色气体,在液面上方变为红棕色. |
| 实验Ⅱ | 15mol•L-1浓硝酸 | 电流计指针先向右偏转,很快又偏向左边,铝片和铜片表面产生红棕色气体,溶液变为绿色. |
(2)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是Al开始作电池的负极,Al在浓硝酸中迅速生成致密氧化膜后,Cu作负极.
查阅资料:活泼金属与1mol•L-1稀硝酸反应有H2和NH4+生成,NH4+生成的原理是产生H2的过程中NO3-被还原.
 (3)用如图装置进行实验Ⅲ:溶液X为1mol•L-1稀硝酸溶液,观察到电流计指针向右偏转.
(3)用如图装置进行实验Ⅲ:溶液X为1mol•L-1稀硝酸溶液,观察到电流计指针向右偏转.①反应后的溶液中含NH4+.实验室检验NH4+的方法是取少量待检溶液于试管中,加入浓NaOH溶液,加热,若产生使湿润的红色石蕊试纸变蓝的气体,则溶液中含NH4+.
②生成NH4+的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(4)进一步探究碱性条件下NO3-的氧化性,进行实验Ⅳ:
①观察到A中有NH3生成,B中无明显现象.A、B产生不同现象的解释是Al与NaOH溶液反应产生H2的过程中可将NO3-还原为NH3,而Mg不能与NaOH.
②A中生成NH3的离子方程式是8Al+3NO3-+5OH-+2H2O=3NH3↑+8AlO2-.
(5)将铝粉加入到NaNO3溶液中无明显现象,结合实验Ⅲ和Ⅳ说明理由因为铝与中性的硝酸钠溶液无生成H2的过程,NO3-无法被还原.
 2NH3.
2NH3.