4.利用催化技术可将汽车尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
下列说法中,不正确的是( )
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/×10-3 mol•L-1 | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
| c(CO)/×10-3 mol•L-1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
| A. | 2s内的平均反应速率υ(N2)=1.875×10-4mol•L-1•s-1 | |
| B. | 在该温度下,反应的平衡常数K=5 | |
| C. | 若将容积缩小为原来的一半,NO转化率大于90% | |
| D. | 使用催化剂可以提高单位时间CO和NO的处理量 |
3.已知氯水中存在反应:Cl2+H2O?H++Cl-+HClO,取5mL饱和氯水进行如下实验.下列说法中,正确的是( )
| A. | 加5 mL水,c (H+)增大 | B. | 加少量NaCl固体,c (H+)不变 | ||
| C. | 加少量碳酸钙粉末,c(HClO)升高 | D. | 加少量Na2SO3固体,溶液pH升高 |
2.常温下,下列各组离子在指定溶液中,一定可以大量共存的是( )
| A. | 无色溶液中 Mg2+、Al3+、SO42-、CO32- | |
| B. | pH=1的溶液中 NH4+、Ba2+、HCO3-、NO3- | |
| C. | 含MnO4-的溶液中 H+、K+、Br-、I- | |
| D. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12的溶液中 Na+、K+、CH3COO-、SO42- |
1.下列说法中,不正确的是( )
| A. | 麦芽糖水解的产物只有葡萄糖 | |
| B. | 苯酚可用于合成高分子化合物 | |
| C. | 油脂水解可以制取高级脂肪酸 | |
| D. | 鸡蛋清遇醋酸铅后产生的沉淀能重新溶于水 |
20.酸雨形成的示意图如图.下列说法中,不正确的是( )
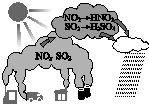

| A. | 汽车尾气是导致酸雨的原因之一 | B. | 酸雨会使土壤、湖泊酸化 | ||
| C. | 酸雨形成中不涉及氧化还原反应 | D. | 燃煤中加入石灰石可防治酸雨 |
19.下列化学用语正确的是( )
| A. | 丙烯的实验式 C3H6 | |
| B. | 镁离子的结构示意图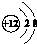 | |
| C. | CO2的电子式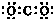 | |
| D. | 中子数为18的氯原子符号${\;}_{17}^{18}$Cl |
18.化学与日常生活紧密相关.下列说法中,不正确的是( )
| A. | 甲醛可作食品防腐剂 | B. | 氢氧化铝可作抗酸药 | ||
| C. | 氯化钠可作食品调味剂 | D. | 生石灰可作食品干燥剂 |
17.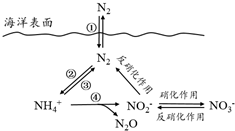 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用如图表示.
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用如图表示.
(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是②(填图中数字序号).
(2)下列关于海洋氮循环的说法正确的是ad(填字母序号).
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO3-的废水会影响海洋中NH4+的含量
(3)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:
NH4++5O2═2NO2-+6H++N2O+5H2O
(4)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10L人工海水样本的监测数据:
硝化细菌去除氨氮的最佳反应温度是25℃,在最佳反应温度时,48h内去除氨氮反应的平均速率是1.125mg•L-1•h-1.
(5)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放.图是间接氧化工业废水中氨氮(NH4+)的示意图.
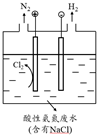
①结合电极反应式简述间接氧化法去除氨氮的原理:阳极反应2Cl--2e-=Cl2,产生的Cl2氧化废水中的NH4+释放出N2.
②若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将减小(填“增大”、“不变”或“减小”),请简述理由:电路中通过相同电量时,若生成n(H2):n(N2)=3:1,则阳极产生的H+比阴极消耗的H+多.
0 152601 152609 152615 152619 152625 152627 152631 152637 152639 152645 152651 152655 152657 152661 152667 152669 152675 152679 152681 152685 152687 152691 152693 152695 152696 152697 152699 152700 152701 152703 152705 152709 152711 152715 152717 152721 152727 152729 152735 152739 152741 152745 152751 152757 152759 152765 152769 152771 152777 152781 152787 152795 203614
 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用如图表示.
氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用如图表示.(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是②(填图中数字序号).
(2)下列关于海洋氮循环的说法正确的是ad(填字母序号).
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO3-的废水会影响海洋中NH4+的含量
(3)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:
NH4++5O2═2NO2-+6H++N2O+5H2O
(4)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10L人工海水样本的监测数据:
| 温度/℃ | 样本氨氮含量/mg | 处理24h | 处理48h |
| 氨氮含量/mg | 氨氮含量/mg | ||
| 20 | 1008 | 838 | 788 |
| 25 | 1008 | 757 | 468 |
| 30 | 1008 | 798 | 600 |
| 40 | 1008 | 977 | 910 |
(5)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放.图是间接氧化工业废水中氨氮(NH4+)的示意图.

①结合电极反应式简述间接氧化法去除氨氮的原理:阳极反应2Cl--2e-=Cl2,产生的Cl2氧化废水中的NH4+释放出N2.
②若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将减小(填“增大”、“不变”或“减小”),请简述理由:电路中通过相同电量时,若生成n(H2):n(N2)=3:1,则阳极产生的H+比阴极消耗的H+多.


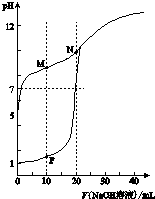 用0.1mol•L-1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1mol•L-1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图:
用0.1mol•L-1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1mol•L-1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图: