9. 自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
(1)反应需要在闪电或极高温条件下发生,说明该反应A.(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)?2NO(g)的平衡常数K如下表:
①该反应的△H>0.(填“>”、“=”或“<”)
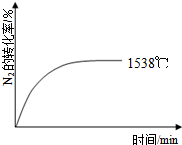
②其他条件相同时,在上述三个温度下分别发生该反应.1538℃时,N2的转化率随时间变化如右图所示,请补充完成1760℃、2404℃时N2的转化率随时间变化的示意图.
(3)一定条件下该反应在密闭容器中达到平衡后,要提高N2的转化率,可以采取的措施是AE.
A.降低温度 B.加催化剂 C.增加压强
D.增加O2浓度 E.分离出一氧化氮
(4)NO在科学界被誉为“明星分子”,用NO与O2反应可以制备NO2,NO2是一种优良的氧化剂.已知火箭发射时可用肼(N2H4)作燃料,NO2作氧化剂,这两者反应生成N2和H2O(气).
且:N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ/mol
请写出肼与NO2反应的热化学方程式2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol.
 自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.(1)反应需要在闪电或极高温条件下发生,说明该反应A.(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)?2NO(g)的平衡常数K如下表:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
②其他条件相同时,在上述三个温度下分别发生该反应.1538℃时,N2的转化率随时间变化如右图所示,请补充完成1760℃、2404℃时N2的转化率随时间变化的示意图.
(3)一定条件下该反应在密闭容器中达到平衡后,要提高N2的转化率,可以采取的措施是AE.
A.降低温度 B.加催化剂 C.增加压强
D.增加O2浓度 E.分离出一氧化氮
(4)NO在科学界被誉为“明星分子”,用NO与O2反应可以制备NO2,NO2是一种优良的氧化剂.已知火箭发射时可用肼(N2H4)作燃料,NO2作氧化剂,这两者反应生成N2和H2O(气).
且:N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ/mol
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534kJ/mol
请写出肼与NO2反应的热化学方程式2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=-1135.7KJ/mol.
8. (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示正反应程度越大反应进行越完全,反应的转化率越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示正反应程度越大反应进行越完全,反应的转化率越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).
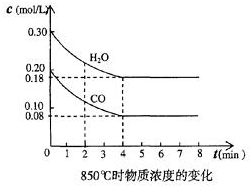
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)?CO2(g)十H2 (g)十Q(Q>0)
CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03 mol/(L•min)
t1时物质浓度(mol/L)的变化
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表.
①表中3min~4min之间反应处于平衡状态;C1数值大于0.08mol/L (填大于、小于或等于).
②反应在4min~5min问,平衡向逆方向移动,可能的原因是d(单选),表中5min~6min之间数值发生变化,可能的原因是a(单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
 (1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示正反应程度越大反应进行越完全,反应的转化率越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示正反应程度越大反应进行越完全,反应的转化率越大,K值大小与温度的关系是:温度升高,K值可能增大也可能减小(填一定增大、一定减小、或可能增大也可能减小).(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)?CO2(g)十H2 (g)十Q(Q>0)
CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03 mol/(L•min)
t1时物质浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.38 | 0.238 | 0.062 | 0.062 |
| 3 | c | c2 | c3 | c3 |
| 4 | c | c2 | c3 | c3 |
| 5 | 0.6 | 0.26 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
①表中3min~4min之间反应处于平衡状态;C1数值大于0.08mol/L (填大于、小于或等于).
②反应在4min~5min问,平衡向逆方向移动,可能的原因是d(单选),表中5min~6min之间数值发生变化,可能的原因是a(单选).
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
7.pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是( )
| A. | 反应开始时的速率:甲=乙 | |
| B. | 反应所需时间:甲<乙 | |
| C. | 反应开始时,酸的物质的量浓度:乙<甲 | |
| D. | 反应结完后溶液的pH值:甲<乙 |
6.关于水的离子积常数,下列说法中不正确的是( )
| A. | 纯水中c(H+)•c(OH-)=1×10-14 | B. | 25℃纯水中c(H+)•c(OH-)=1×10-14 | ||
| C. | 25℃稀盐酸中c(H+)•c(OH-)=1×10-14 | D. | KW值随温度升高而增大 |
5.下列说法正确的是( )
| A. | 物质发生化学变化都伴随着能量变化 | |
| B. | 任何反应中的能量变化都表现为热量变化 | |
| C. | 伴有能量变化的物质变化都是化学变化 | |
| D. | 所有化学反应都可以设计成原电池 |
2.X、Y、Z、W均是周期表中短周期元素,原子序数逐渐增大,有关信息如下:
(1)甲是X的最高价氧化物,X的最高正价是+4,甲的电子式为 ,X的气态氢化物电子式为
,X的气态氢化物电子式为 .
.
(2)W在元素周期表的位置第三周期第ⅦA族,用电子式表示化合物YW的形成过程
(3)乙是Y的最高价氧化物对应水化物,写出下列反应离子方程式:
①过量的甲通入乙溶液中CO2+OH-=HCO3-
②Z的单质和乙溶液反应2Al+2OH-+2H2O=2AlO2-+3H2↑
③W的单质与乙溶液反应Cl2+2OH-=Cl-+ClO-+H2O.
| 元素 | 相关信息 |
| X | X的原子L层电子数是K层电子数的2倍 |
| Y | Y是短周期元素中原子半径最大的元素(除稀有气体元素外) |
| Z | Z的原子最外层电子数等于电子层数 |
| W | W原子最外层电子数是X、Z原子最外层电子数之和 |
 ,X的气态氢化物电子式为
,X的气态氢化物电子式为 .
.(2)W在元素周期表的位置第三周期第ⅦA族,用电子式表示化合物YW的形成过程

(3)乙是Y的最高价氧化物对应水化物,写出下列反应离子方程式:
①过量的甲通入乙溶液中CO2+OH-=HCO3-
②Z的单质和乙溶液反应2Al+2OH-+2H2O=2AlO2-+3H2↑
③W的单质与乙溶液反应Cl2+2OH-=Cl-+ClO-+H2O.
1.下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)⑥的最低负价是-2;⑦的最高价含氧酸的化学式为HClO4.
(2)③、④、⑦的简单离子半径由大到小的顺序为Cl->F->Na+用离子符号表示).
(3)⑦的单质电子式为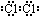 ,由②、④两种元素的原子按1:1组成化合物的电子式为
,由②、④两种元素的原子按1:1组成化合物的电子式为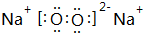 .
.
(4)②、⑥的单质中更易与①的单质反应的是氧气,用原子结构的理论解释原因是同一主族从上到下,原子半径增大,得电子能力减弱,元素的非金属减弱,所以氧气的氧化性比硫强.
(5)④、⑤的最高价氧化物对应水化物之间发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)若用①、②的单质和④的最高价氧化物对应水化物的溶液设计成化学电源,则该电池负极的电极反应式为H2+2OH--2e-=2H2O正极的电极反应式为O2+2H2O+4e-=4OH-.
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(2)③、④、⑦的简单离子半径由大到小的顺序为Cl->F->Na+用离子符号表示).
(3)⑦的单质电子式为
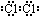 ,由②、④两种元素的原子按1:1组成化合物的电子式为
,由②、④两种元素的原子按1:1组成化合物的电子式为 .
.(4)②、⑥的单质中更易与①的单质反应的是氧气,用原子结构的理论解释原因是同一主族从上到下,原子半径增大,得电子能力减弱,元素的非金属减弱,所以氧气的氧化性比硫强.
(5)④、⑤的最高价氧化物对应水化物之间发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(6)若用①、②的单质和④的最高价氧化物对应水化物的溶液设计成化学电源,则该电池负极的电极反应式为H2+2OH--2e-=2H2O正极的电极反应式为O2+2H2O+4e-=4OH-.
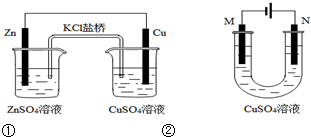
20.关于下列装置的说法正确的是( )
0 152536 152544 152550 152554 152560 152562 152566 152572 152574 152580 152586 152590 152592 152596 152602 152604 152610 152614 152616 152620 152622 152626 152628 152630 152631 152632 152634 152635 152636 152638 152640 152644 152646 152650 152652 152656 152662 152664 152670 152674 152676 152680 152686 152692 152694 152700 152704 152706 152712 152716 152722 152730 203614

| A. | 装置①中盐桥内的K+移向CuSO4溶液 | |
| B. | 装置①将电能转变为化学能 | |
| C. | 若装置②用于铁棒镀铜,则N极为铁棒 | |
| D. | 若装置②用于电解精炼铜,则N极为粗铜 |

 .
.