15.在0.10mol•L-1 NH3•H2O的溶液中,加水稀释后,引起的变化是( )
| A. | 溶液的pH增大 | B. | NH3•H2O的电离平衡常数增大 | ||
| C. | NH3•H2O的电离程度增大 | D. | NH3•H2O溶液中所有离子浓度减小 |
14.将2.1g CO和3.6g H2的混合气体与32g O2充分燃烧,立即通入足量的Na2O2固体中,则固体的质量增重( )
| A. | 2.1g | B. | 3.6g | C. | 5.7g | D. | 37.7g |
13.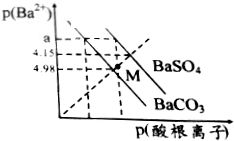 已知:p(Ba2+)=-lgc(Ba2+),p(酸根离子)=-lgc(酸根离子),酸根离子为SO42-或CO32-.某温度下BaSO4、BaCO3的沉淀溶解关系如图所示,下列叙述正确的是( )
已知:p(Ba2+)=-lgc(Ba2+),p(酸根离子)=-lgc(酸根离子),酸根离子为SO42-或CO32-.某温度下BaSO4、BaCO3的沉淀溶解关系如图所示,下列叙述正确的是( )
 已知:p(Ba2+)=-lgc(Ba2+),p(酸根离子)=-lgc(酸根离子),酸根离子为SO42-或CO32-.某温度下BaSO4、BaCO3的沉淀溶解关系如图所示,下列叙述正确的是( )
已知:p(Ba2+)=-lgc(Ba2+),p(酸根离子)=-lgc(酸根离子),酸根离子为SO42-或CO32-.某温度下BaSO4、BaCO3的沉淀溶解关系如图所示,下列叙述正确的是( )| A. | p(Ba2+)=a时,溶液中所含的c(SO42-)>c(CO32-) | |
| B. | M点对应溶液中的Ba2+、CO32-能形成BaCO3沉淀 | |
| C. | 由图可知该温度下,KSP(BaSO4)<KSP(BaCO3) | |
| D. | BaSO4淀不能转化为BaCO3沉淀 |
12.下列关于晶体和非晶体叙述不正确的是( )
| A. | 晶体区别于非晶体的本质特征是晶体中原子呈周期性有序排列 | |
| B. | 缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为的立方体晶体体现了晶体的自范性 | |
| C. | M为第ⅡA元素,MCO3中M2+半径越大,MCO3热分解温度越低 | |
| D. | 干冰中CO2的配位数12大于冰中H2O的配位数4,是由于丙中水分子之间存在氢键 |
10.工业上湿法炼锌过程中.以ZnSO4为主要成分的浸出液中,含有Fe3+、Fe2+、Cu2+、Cl-等杂质,这些杂质对锌的电解工序有妨碍,必须提早除去.现有下列试剂可供选择:①酸性KMnO4溶液、②NaOH溶液、③ZnO、④H2O2溶液、⑤Zn、⑥Fe、⑦AgNO3溶液、⑧Ag2SO4,下列说法不正确的是 ( )
0 152438 152446 152452 152456 152462 152464 152468 152474 152476 152482 152488 152492 152494 152498 152504 152506 152512 152516 152518 152522 152524 152528 152530 152532 152533 152534 152536 152537 152538 152540 152542 152546 152548 152552 152554 152558 152564 152566 152572 152576 152578 152582 152588 152594 152596 152602 152606 152608 152614 152618 152624 152632 203614
| A. | 用酸性KMnO4溶液将Fe2+氧化成Fe3+,再转化为Fe(OH)3沉淀除去 | |
| B. | 用ZnO调节浸出液的酸碱性,可使某些离子形成氢氧化物沉淀 | |
| C. | 在实际生产过程中,加入Ag2SO4可除去Cl-,是利用了沉淀转化的原理 | |
| D. | 也可以用ZnCO3代替ZnO调节溶液的酸碱性 |

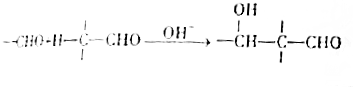
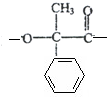
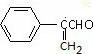 +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$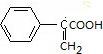 +Cu2O+2H2O
+Cu2O+2H2O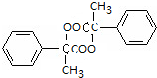
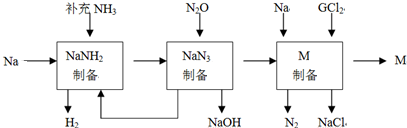

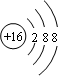 ,32g甲在足量浓硝酸中反应转移的电子数为2NA.
,32g甲在足量浓硝酸中反应转移的电子数为2NA.