18.下列说法不正确的是( )
| A. | 用废弃动植物油脂与低碳醇通过酯交换反应制成生物柴油来代替柴油作为机车燃料,这种做法符合“绿色化学”理念 | |
| B. | 生物炼铜是利用生物质能转化为化学能的原理实现的 | |
| C. | 元素分析仪不但可以检测物质中的许多非金属元素,也可以检测金属元素 | |
| D. | 霾是悬浮在大气中的大量微小尘粒、烟粒或盐粒的集合体,霾的形成与PM2.5有直接关系 |
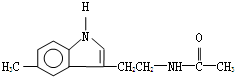
12.脑白金主要成分的结构简式如图所示,下列对脑白金主要成分的推论正确的是( )
0 152377 152385 152391 152395 152401 152403 152407 152413 152415 152421 152427 152431 152433 152437 152443 152445 152451 152455 152457 152461 152463 152467 152469 152471 152472 152473 152475 152476 152477 152479 152481 152485 152487 152491 152493 152497 152503 152505 152511 152515 152517 152521 152527 152533 152535 152541 152545 152547 152553 152557 152563 152571 203614

| A. | 其官能团和营养成分与葡萄糖相同 | |
| B. | 其分子式为C13H15N2O | |
| C. | 该物质不能与溴的四氯化碳溶液反应 | |
| D. | 该物质能发生水解反应并生成乙酸 |
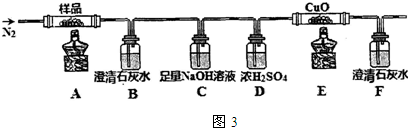
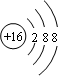 ;32g甲在足量浓硝酸中反应转移的电子数为2NA;甲在足量氧气中充分灼烧的化学方程式为Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2.
;32g甲在足量浓硝酸中反应转移的电子数为2NA;甲在足量氧气中充分灼烧的化学方程式为Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2.