17.常温下,将0.1000mol•L-1NaOH溶液滴入20.0mL0.1000mol•L-1的一元酸HA溶液中,测得混合溶液的PH变化曲线如图所示,下列说法正确的是( )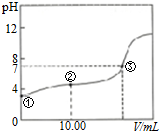

| A. | 两溶液反应的离子方程式是H++OH-+H2O | |
| B. | 图中②点所示溶液中:2c(Na+)=c(HA)+c(A-) | |
| C. | 图中②点所示溶液中:c(A-)>c(H+)>c(HA)>c(OH-) | |
| D. | 图中③点所示滴入的NaOH溶液的体积V=20.00mL |
16.在密闭容器中发生反应:X+3Y?2Z(g),其中Z是平衡混合气中的体积分数(Z%)与温度(T)、压强(p)的关系如图,速率判断正确的是( )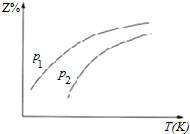
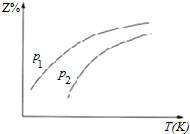
| A. | △H<0 | |
| B. | 若p1>p2,则Y一定呈气态 | |
| C. | 升高温度,该反应的化学平衡常数减小 | |
| D. | 反应处于平衡状态时,有c(X):c(2)=1:2 |
15.下列实验操作与预期目的或所得实验结论一致的是( )
| 选项 | 实验操作 | 实验目的或结论 |
| A | 向1mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下,溶解度:Mg(OH)2>Fe(OH)3 |
| B | 向两份等体积等浓度的H2O2溶液中,分别滴入等浓度等体积CuSO4、KMnO4溶液,后者产生气体较多 | 证明KMnO4溶液的催化效率更高 |
| C | 测定相同物质的量浓度的硅酸钠 和碳酸钠溶液的PH,前者较大 | 证明非金属性:C>Si |
| D | 向FeCl3溶液中加入铁钉,溶液颜色变浅 | 证明FeCl3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
14.有关如图所示原电池的叙述正确的是( )
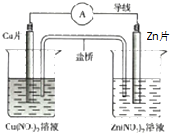

| A. | 盐桥中阴离子向正极移动 | |
| B. | 正极的电极反应是:Zn2++2e-═Zn | |
| C. | Zn片上发生氧化反应 | |
| D. | 用该电池电解水,析出3.2gCu时生成1.12LO2(标况下) |
13.下列反应的离子方程式书写正确的是( )
| A. | AlCl3溶液中加入过量氨水:Al3++4NH3•H2O═AlO${\;}_{2}^{-}$+4NH${\;}_{4}^{+}$+2H2O | |
| B. | 在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+H2O2+2H+═I2+O2↑+2H2O | |
| C. | 在氢氧化钡溶液中滴加硫酸氢钾溶液至PH=7:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| D. | 用碳酸钠溶液浸泡锅炉水垢:Ca2++CO32-═CaCO3↓ |
12.4种短周期元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为15,W的最高价与最低价代数和为0,Y是同周期元素中离子半径最小的,Y、Z原子序数之差为4,下列说法不正确的是( )
| A. | X是短周期元素中原子半径最大的 | |
| B. | X元素最高价氧化物对应的水化物,可以与其他三种元素最高价氧化物对应的水化物反应 | |
| C. | WZ4分子中每个原子最外层均达到8电子结构 | |
| D. | X元素的氧化物中只存在离子键 |
11.下列有关环境污染的叙述不正确的是( )
| A. | 使用无磷洗衣粉,可彻底解决水体富营养化问题 | |
| B. | SO2是大气污染物,可以用生石灰除去工业废气中的SO2 | |
| C. | 明矾水解产生Al(OH)3胶体粒子,可除去悬浮物 | |
| D. | 使用清洁能源是防止酸雨发生的重要措施之一 |
9.Ⅰ.现有浓度均为0.1mol•L -1的下列溶液:
①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨
水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)④②③①.
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)⑥⑦④⑤⑧.
(3)将③和④等体积混合后,混合液中各离子浓度关系正确的是A.
A.c(Na+)=c(C1-)>c(OH-)>c(NH4+)
B.c(Na+)=0.1mol•L-1
C.c(Na+)+c(NH4+)=c(C1-)+c(OH-)
D.c(H+)>c(OH-)
Ⅱ.如表是不同温度下水的离子积的数据:
试回答以下问题:
(1)若25<t l<t 2,则a>1×10-14(填“>”、“<”或“=”),做此判断的理由是水的电离为吸热反应,升高温度,平衡向着正反应方向移动.
(2)25℃时,某Na2S04溶液中c(S042-)=5×10-4 mol•L-1,取该溶液l mL加水稀释至10mL,则
稀释后溶液中c(Na+):c(OH-)=1000:1.
(3)在t2温度下,将pH=11的NaOH溶液a L与pH=1的H2S04溶液b L混合,若所得混合液pH=2,则a:b=9:11.
0 152355 152363 152369 152373 152379 152381 152385 152391 152393 152399 152405 152409 152411 152415 152421 152423 152429 152433 152435 152439 152441 152445 152447 152449 152450 152451 152453 152454 152455 152457 152459 152463 152465 152469 152471 152475 152481 152483 152489 152493 152495 152499 152505 152511 152513 152519 152523 152525 152531 152535 152541 152549 203614
①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨
水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)④②③①.
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)⑥⑦④⑤⑧.
(3)将③和④等体积混合后,混合液中各离子浓度关系正确的是A.
A.c(Na+)=c(C1-)>c(OH-)>c(NH4+)
B.c(Na+)=0.1mol•L-1
C.c(Na+)+c(NH4+)=c(C1-)+c(OH-)
D.c(H+)>c(OH-)
Ⅱ.如表是不同温度下水的离子积的数据:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
(1)若25<t l<t 2,则a>1×10-14(填“>”、“<”或“=”),做此判断的理由是水的电离为吸热反应,升高温度,平衡向着正反应方向移动.
(2)25℃时,某Na2S04溶液中c(S042-)=5×10-4 mol•L-1,取该溶液l mL加水稀释至10mL,则
稀释后溶液中c(Na+):c(OH-)=1000:1.
(3)在t2温度下,将pH=11的NaOH溶液a L与pH=1的H2S04溶液b L混合,若所得混合液pH=2,则a:b=9:11.

