9.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在0.1molNaHSO4晶体中阳离子与阴离子总数为0.3NA | |
| B. | 1.0L0.1mol•L-1NH4NO3溶液中含有的铵根离子数是0.1×6.02×1023 | |
| C. | 7.8gNa2O2与足量CO2反应,转移的电子数为0.1NA | |
| D. | 向仅含0.2molFeI2的溶液中持续通入氯气,当有0.1molFe2+被氧化时,需通入标况下C121.12L |
6.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1L2mol•L-1的(NH4)2S溶液中含有的S2-数目为0.2NA | |
| B. | 7.8g苯中含有C=C键数目为0.3NA | |
| C. | 常温常压下,5.6g乙烯和环丙烷的混合气体中含有的碳原子数为0.4NA | |
| D. | 用惰性电极电解1L浓度均为2mol•L-1的AgNO3与Cu(NO3)2的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 |
5.下列离子方程式正确的是( )
| A. | 氨水与稀盐酸反应:H++OH-═H2O | |
| B. | FeCl3溶液与铁反应:Fe3++Fe═2Fe2+ | |
| C. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| D. | KOH稀溶液中通入过量的SO2:SO2+OH-═HSO3- |
2.下表是五种主族元素的结构特点及其元素、单质、化合物的性质.
(1)写出X元素的原子核外电子排布1s22s22p3;其单质的化学性质稳定(填“稳定”或“活泼”),该元素的非金属性强(填“强”或“弱”),证明其强弱的理由是硝酸是强酸.
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式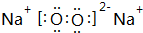 ;已知w 的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为分子晶体.
;已知w 的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为分子晶体.
(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:Al(OH)3+3H+=Al3++3H2O,Al(OH)3+OH-=AlO2-+2H2O.
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为AB.
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.
| 元素 | 结构特点及元素、单质、化合物的性质 |
| X | 气态氢化物与最高价氧化物对应水化物可以化合成盐 |
| Y | 原子中s电子数与p电子数相同,且p电子的能量最高 |
| Z | 单质在空气中燃烧产生黄色火焰,生成黄色粉末 |
| W | 最外层电子排布(n+1)sn(n+1)pn-1 |
| T | 单质升华可以产生紫色的烟 |
(2)Z单质在空气中燃烧生成黄色粉末,写出该物质的电子式
 ;已知w 的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为分子晶体.
;已知w 的氯化物在177.8°C时会发生升华现象,由此可以判断它的晶体类型为分子晶体.(3)W的最高价氧化物对应水化物可以与X、Z的最高价氧化物对应水化物反应,写出反 应的离子方程式:Al(OH)3+3H+=Al3++3H2O,Al(OH)3+OH-=AlO2-+2H2O.
(4)一种元素有多种可变价态,一般高价氧化物对应水化物成酸,低价氧化物对应水化物成碱.Y、T可形成多种化合物,其中T元素的化合价为+3、+5时,形成的化合物的化学式为AB.
A.T2Y4 B.T4Y9 C.T6Y10 D.T2Y3.
1.下列反应的离子方程式正确的是( )
0 152282 152290 152296 152300 152306 152308 152312 152318 152320 152326 152332 152336 152338 152342 152348 152350 152356 152360 152362 152366 152368 152372 152374 152376 152377 152378 152380 152381 152382 152384 152386 152390 152392 152396 152398 152402 152408 152410 152416 152420 152422 152426 152432 152438 152440 152446 152450 152452 152458 152462 152468 152476 203614
| A. | 纯碱溶液中加入苯酚:CO32-+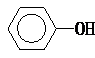 → →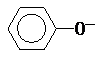 +HCO3- +HCO3- | |
| B. | 小苏打溶液中加醋酸溶液:HCO3-+CH3COOH→CO2↑+CH3COO- | |
| C. | 明矾溶液中加入过量的Ba(OH)2溶液:Al3++4OH-→AlO2-+2H2O | |
| D. | 氯化铵溶于水:NH4++2H2O?H3O++NH3•H2O |

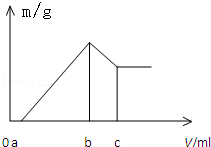 将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:
将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算: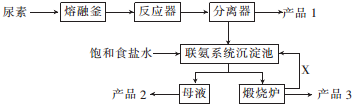
 ,请回答下列问题:
,请回答下列问题: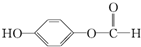 .
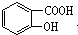
.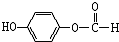 ,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)C;
,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)C;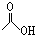 ,在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林可表示为:
,在一定条件下,水杨酸与乙酸酐可合成阿斯匹林,阿斯匹林可表示为: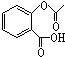 ,则阿斯匹林的分子式为C9H8O4.
,则阿斯匹林的分子式为C9H8O4. .
.