6.常温下,浓度均为0.1mol/L的四种溶液pH如下表,下列说法中正确的是( )
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 8.3 | 10.7 | 4.0 |
| A. | 0.1 mol/L Na2CO3溶液加水,稀释后溶液中所有离子的浓度均减少 | |
| B. | NaHCO3溶液中2c(H2CO3)+c(H+)=c(OH-)+c(CO32-) | |
| C. | NaHSO3溶液中c(Na+)>c(HSO3-)>c(H2SO3)>c(SO32-)>c(H+)>c(OH-) | |
| D. | 向NaClO溶液中滴加硫酸至中性时,2c(SO42-)=c(HClO) |
4.解释下列现象的化学用语正确的是( )
| A. | 铁钉在空气中出现红色的铁锈,其负极反应式为:Fe-3e-═Fe3+ | |
| B. | 氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+NH4+═Mg2++NH3•H2O | |
| C. | 向足量铝粉与氢氧化钠溶液反应后的溶液中滴加碳酸氢钠溶液:HCO3-+AlO2-+H2O═Al(OH)3↓+CO32- | |
| D. | 漂白粉溶液中加氯化亚铁溶液产生大量沉淀:Fe2++2ClO-+2H2O═Fe(OH)2↓+2HClO |
3.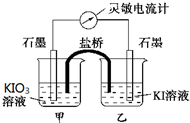 将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池,甲、乙烧杯中都加入淀粉溶液.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转.下列判断不正确的是( )
将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池,甲、乙烧杯中都加入淀粉溶液.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转.下列判断不正确的是( )
 将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池,甲、乙烧杯中都加入淀粉溶液.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转.下列判断不正确的是( )
将反应IO3-+5I-+6H+?3I2+3H2O设计成如图所示的原电池,甲、乙烧杯中都加入淀粉溶液.开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转.下列判断不正确的是( )| A. | 两次电流计指针偏转方向相反,电流计读数为零时,反应达到化学平衡状态 | |
| B. | 两次实验中,盐桥中的阳离子移动方向相反 | |
| C. | 开始加入少量浓硫酸时,只有乙烧杯中溶液变蓝 | |
| D. | 向甲烧杯中滴入几滴浓NaOH溶液后,乙中石墨电极上发生还原反应 |
2. 向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用如图简单表示(“-”表示铁各种价态的变化,用“-•-”表示碘各种形态的变化).下列结论错误的是( )
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用如图简单表示(“-”表示铁各种价态的变化,用“-•-”表示碘各种形态的变化).下列结论错误的是( )
 向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用如图简单表示(“-”表示铁各种价态的变化,用“-•-”表示碘各种形态的变化).下列结论错误的是( )
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用如图简单表示(“-”表示铁各种价态的变化,用“-•-”表示碘各种形态的变化).下列结论错误的是( )| A. | Cl2、I2、IO3-、Fe3+的氧化性依次减小 | |
| B. | 当$\frac{n(C{l}_{2})}{n(Fe{I}_{2})}$=1.2时,反应的离子方程式为2Fe2++10I-+6Cl2═5I2+2Fe3++12Cl- | |
| C. | 当$\frac{n(C{l}_{2})}{n(Fe{I}_{2})}$=6.5时,溶液中$\frac{n(C{l}^{-})}{n(I{O}_{3}^{-})}$=6.5 | |
| D. | 若溶液的体积不变,则溶液的pH减小 |
1.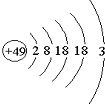 张青莲是我国著名的化学家.1991年,他准确测得In的相对原子质量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中首次采用我国测定的相对原子质量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
张青莲是我国著名的化学家.1991年,他准确测得In的相对原子质量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中首次采用我国测定的相对原子质量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
 张青莲是我国著名的化学家.1991年,他准确测得In的相对原子质量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中首次采用我国测定的相对原子质量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )
张青莲是我国著名的化学家.1991年,他准确测得In的相对原子质量为114.818,被国际原子量委员会采用为新的标准值.这是原子量表中首次采用我国测定的相对原子质量值.已知In的原子结构如图所示,则下列关于In的说法不正确的是( )| A. | In为长周期元素 | B. | In为过渡金属元素 | ||
| C. | In容易导电导热 | D. | In在反应中容易失电子 |
20. 甲~庚元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断不正确的是( )
甲~庚元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断不正确的是( )
 甲~庚元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断不正确的是( )
甲~庚元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断不正确的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 气态氢化物的稳定性:庚>己>戊 | |
| C. | 丁的氧化物可用于制造光导纤维 | |
| D. | 常温下,甲和乙的单质均能与水剧烈反应 |
18.碳酸锰,俗称“锰白”,是生产电讯器材软磁铁氧体的原料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,工业上有广泛的用途.工业上以软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2)为主要原料制备碳酸锰(MnCO3难溶,分解温度较高)的一种工艺流程如图1:

已知:几种金属离子沉淀的pH如表回答下列问题:
(1)为了提高溶浸工序中原料的浸出效率,可以采取的措施有ABC.
A.适当升高温度 B.适当增大压强
C.研磨矿石 D.加入大量的蒸馏水
(2)溶浸过程中发生的主要反应是:FeS2与MnO2在稀硫酸中反应生成Fe3+、Mn2+、SO42-和H2O.在该反应配平的离子方程式中,氧化剂前面的化学计量数为15.
(3)除铁工序中,①先加入软锰矿,反应的离子方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;
②再加入石灰的目的是3.7~5.2.
(4)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质.若测得滤液中c(Fˉ)=0.01mol•L-1,滤液中残留c(Ca2+)=1.5×10ˉ6mol•L-1,则Ksp(CaF2)=1.5×10ˉ10(mol3•L-3).
(5)沉锰工序中,298K、c(Mn2+)为1.05mol•L-1时,实验测得MnCO3的产率与溶液的pH、反应时间关系如图2所示.对比不同反应条件下的曲线,依据图中信息,你能获得的结论有:
①pH等于7.0时反应速率最快,且MnCO3产率最高;②pH越大越有利于提升MnCO3的产率.
(6)副产品A的主要成分是(NH4)2SO4.
0 152271 152279 152285 152289 152295 152297 152301 152307 152309 152315 152321 152325 152327 152331 152337 152339 152345 152349 152351 152355 152357 152361 152363 152365 152366 152367 152369 152370 152371 152373 152375 152379 152381 152385 152387 152391 152397 152399 152405 152409 152411 152415 152421 152427 152429 152435 152439 152441 152447 152451 152457 152465 203614

已知:几种金属离子沉淀的pH如表回答下列问题:
| Fe2+ | Fe3+ | Cu2+ | Mn2+ | |
| 开始沉淀的pH | 7.5 | 3.2 | 5.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 7.8 | 10.4 |
A.适当升高温度 B.适当增大压强
C.研磨矿石 D.加入大量的蒸馏水
(2)溶浸过程中发生的主要反应是:FeS2与MnO2在稀硫酸中反应生成Fe3+、Mn2+、SO42-和H2O.在该反应配平的离子方程式中,氧化剂前面的化学计量数为15.
(3)除铁工序中,①先加入软锰矿,反应的离子方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;
②再加入石灰的目的是3.7~5.2.
(4)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质.若测得滤液中c(Fˉ)=0.01mol•L-1,滤液中残留c(Ca2+)=1.5×10ˉ6mol•L-1,则Ksp(CaF2)=1.5×10ˉ10(mol3•L-3).
(5)沉锰工序中,298K、c(Mn2+)为1.05mol•L-1时,实验测得MnCO3的产率与溶液的pH、反应时间关系如图2所示.对比不同反应条件下的曲线,依据图中信息,你能获得的结论有:
①pH等于7.0时反应速率最快,且MnCO3产率最高;②pH越大越有利于提升MnCO3的产率.
(6)副产品A的主要成分是(NH4)2SO4.

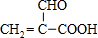
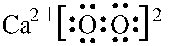 ;加热过氧化钙可分解生成CaO和O2,该反应的化学方程式为2CaO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+O2↑.
;加热过氧化钙可分解生成CaO和O2,该反应的化学方程式为2CaO2$\frac{\underline{\;\;△\;\;}}{\;}$2CaO+O2↑.