12.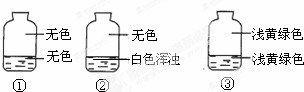 向盛有氯气的三个集气瓶中,分别注入约五分之一的下列液体并振荡,观察如图所记录的现象,判断各瓶注入的液体依次是什么.( )
向盛有氯气的三个集气瓶中,分别注入约五分之一的下列液体并振荡,观察如图所记录的现象,判断各瓶注入的液体依次是什么.( )
 向盛有氯气的三个集气瓶中,分别注入约五分之一的下列液体并振荡,观察如图所记录的现象,判断各瓶注入的液体依次是什么.( )
向盛有氯气的三个集气瓶中,分别注入约五分之一的下列液体并振荡,观察如图所记录的现象,判断各瓶注入的液体依次是什么.( )| A. | AgNO3溶液、NaOH溶液、水 | B. | NaOH溶液、AgNO3溶液、水 | ||
| C. | 水、AgNO3溶液、NaOH溶液 | D. | AgNO3溶液、水、NaOH溶液 |
11.下列有关物质的分类正确的是( )
| A. | CaCl2、NaOH、HCl、HD四种物质都属于化合物 | |
| B. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| C. | 溶液,浊液,胶体都属于混合物 | |
| D. | CO2、CO等非金属氧化物均属于酸性氧化物 |
9.反应A(g)+3B(g)?2C(g)+2D(g)分别从下列两条途径建立平衡:Ⅰ.A、B的起始物质的量分别为2mol和6mol;Ⅱ.C、D的起始物质的量均为2mol.在温度、压强恒定的条件下,以下叙述中不正确的是( )
| A. | Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同 | |
| B. | 达平衡时,途径Ⅰ所得混合气体的密度为途径Ⅱ所得混合气体密度的$\frac{1}{2}$ | |
| C. | 达平衡时,途径Ⅰ的反应速率v(A)等于途径Ⅱ的反应速率v(A) | |
| D. | Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的平均相对分子质量相同 |
8.某恒容密闭容器中充入一定量SO2和O2进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0,反应速率(v)与温度(T)、SO2的体积分数[V(SO2)%]与压强(p)的关系分别如图甲、图乙所示.下列说法正确的是( )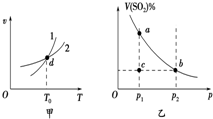

| A. | 图甲中,曲线1表示正反应速率和温度的关系,曲线2表示逆反应速率与温度的关系 | |
| B. | 图乙中,温度恒定时,a、b两点对应的反应速率:va>vb | |
| C. | 图甲中,d点表示温度为T0时,反应已经达到平衡 | |
| D. | 图乙中,温度恒定时,c点的反应正在向正反应方向进行 |
7.已知四种白色粉末分别是硝酸钾、氯化镁、氢氧化钡、无水硫酸铜中的一种.现只提供蒸馏水一种试剂,对这些物质进行鉴别(被鉴别出的物质可作为试剂来鉴别其他物质).请按要求填写下列表格:(注意:用化学式填写)
(1)步骤1:
(2)步骤2:
(3)步骤3:
(1)步骤1:
| 加入试剂 | 被检出物质 | 理由 |
| 水 | CuSO4 | CuSO4溶于水溶液显蓝色 |
| 加入试剂 | 被检出物质 | 离子方程式 |
| CuSO4 |
| 加入试剂 | 被检出物质 | 离子方程式 |
| MgCl2 |
5.现有失去标签的四瓶无色溶液分别为Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示.
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4═Na++H++SO42-.
根据实验现象,回答下列问题:
(1)A为Na2CO3溶液,C为稀盐酸.
(2)写出下列反应的离子方程式
A+BCO32-+Ba2+=BaCO3↓,A+DCO32-+2H+=CO2↑+H2O,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为Ba2++OH-+H++SO42-=BaSO4↓+H2O,反应后得到的溶液中含有的阴离子有OH-.
(4)上述没有明显变化的实验④、⑥,其中④发生了离子反应,离子方程式为H++OH-=H2O.请设计实验证明其发生了反应取少量Ba(OH)2溶液滴入几滴酚酞试液,溶液显红色,向该红色溶液中加入稀盐酸至过量,溶液变为无色,说明酸碱发生反应.(试剂任选)
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 生成白色沉淀 |
| ② | A+C | 放出无色气体 |
| ③ | A+D | 放出无色气体 |
| ④ | B+C | 无明显变化 |
| ⑤ | B+D | 生成白色沉淀 |
| ⑥ | C+D | 无明显变化 |
根据实验现象,回答下列问题:
(1)A为Na2CO3溶液,C为稀盐酸.
(2)写出下列反应的离子方程式
A+BCO32-+Ba2+=BaCO3↓,A+DCO32-+2H+=CO2↑+H2O,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为Ba2++OH-+H++SO42-=BaSO4↓+H2O,反应后得到的溶液中含有的阴离子有OH-.
(4)上述没有明显变化的实验④、⑥,其中④发生了离子反应,离子方程式为H++OH-=H2O.请设计实验证明其发生了反应取少量Ba(OH)2溶液滴入几滴酚酞试液,溶液显红色,向该红色溶液中加入稀盐酸至过量,溶液变为无色,说明酸碱发生反应.(试剂任选)
4.某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法不正确的是( )
0 152190 152198 152204 152208 152214 152216 152220 152226 152228 152234 152240 152244 152246 152250 152256 152258 152264 152268 152270 152274 152276 152280 152282 152284 152285 152286 152288 152289 152290 152292 152294 152298 152300 152304 152306 152310 152316 152318 152324 152328 152330 152334 152340 152346 152348 152354 152358 152360 152366 152370 152376 152384 203614
| A. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| B. | 若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 | |
| C. | 该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- | |
| D. | 若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
