10.室温下,下列溶液的离子浓度关系正确的是( )
| A. | pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合c(Na+)+c(H+)=c(OH-)+c( HC2O4-) | |
| B. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| C. | NaHSO4溶液:c(H+)=c(SO42-)十c(OH-) | |
| D. | pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
7.下表是元素周期表的一部分,按要求完成各小题.
(1)元素①的元素符号:Na
(2)元素⑧的单质电子式
(3)元素⑤的原子结构示意图
(4)化学性质最不活泼的元素⑩(填元编号,下同),非金属性最强的元素是⑪.金属
性最强的单质②.
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH.①③⑤三种元素的原子半径由大到小的顺序为Na>Mg>Al.
(6)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为Al2O3+6HCl=2AlCl3+3H2O,与氢氧化钠溶液反应的化学方程式Al2O3+2NaOH=2NaAlO2+H2O.
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 | |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)元素⑧的单质电子式

(3)元素⑤的原子结构示意图

(4)化学性质最不活泼的元素⑩(填元编号,下同),非金属性最强的元素是⑪.金属
性最强的单质②.
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的NaOH.①③⑤三种元素的原子半径由大到小的顺序为Na>Mg>Al.
(6)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为Al2O3+6HCl=2AlCl3+3H2O,与氢氧化钠溶液反应的化学方程式Al2O3+2NaOH=2NaAlO2+H2O.
6.下列说法正确的是( )
| A. | 碱金属的单质中,锂的还原性最强 | |
| B. | 第ⅠA族元素比第ⅡA族元素的金属性强 | |
| C. | 随着核电荷数的递增,卤族元素的气态氢化物的稳定性逐渐减弱 | |
| D. | 随着核电荷数的递增,第三周期元素的氧化物对应的水化物的酸性逐渐增强. |
5.用化学方法不能实现的是( )
| A. | 生成一种新分子 | B. | 生成一种新离子 | ||
| C. | 生成一种新同位素 | D. | 生成一种新单质 |
3.实施以节约能源和减少废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择.化工行业的发展必须符合国家节能减排的总体要求.试运用所学知识,回答下列问题:
(1)已知某温度下某反应的化学平衡常数表达式为:K=$\frac{c({H}_{2}O)}{c(CO)•c({H}_{2})}$,所对应的化学反应方程式为:CO(g)+H2(g)?C(s)+H2O(g).
(2)已知在一定温度下,
①C(s)+CO2(g)?2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:K3=K1×K2,△H3=(a+b)kJ/mol(用含a、b的代数式表示).
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
该反应的正反应方向是放热反应(填“吸热”或“放热”),若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol•L-1,在该条件下,CO的平衡转化率为:75%.
(4)在催化剂存在条件下反应:H2O(g)+CO(g)?CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图1所示:
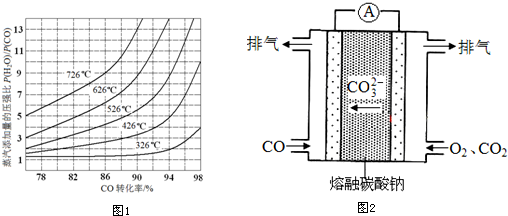
对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=$\frac{P(C{O}_{2})P({H}_{2})}{P(CO)P({H}_{2}O)}$,提高p[H2O(g)]:p(CO)比,则Kp不变(填“变大”、“变小”或“不变”).实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右、p[H2O(g)]:p(CO)=3~5.其原因可能是①该温度下催化剂活性最大②该压强比下,反应物转化率已经接近98%.
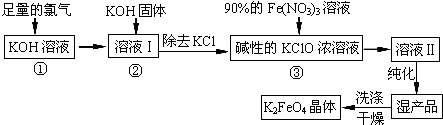
(5)工业上可利用原电池原理除去工业尾气中的CO并利用其电能,反应装置如图2所示,请写出负极的电极反应式:CO-2e-+CO32-=2CO2.
0 152174 152182 152188 152192 152198 152200 152204 152210 152212 152218 152224 152228 152230 152234 152240 152242 152248 152252 152254 152258 152260 152264 152266 152268 152269 152270 152272 152273 152274 152276 152278 152282 152284 152288 152290 152294 152300 152302 152308 152312 152314 152318 152324 152330 152332 152338 152342 152344 152350 152354 152360 152368 203614
(1)已知某温度下某反应的化学平衡常数表达式为:K=$\frac{c({H}_{2}O)}{c(CO)•c({H}_{2})}$,所对应的化学反应方程式为:CO(g)+H2(g)?C(s)+H2O(g).
(2)已知在一定温度下,
①C(s)+CO2(g)?2CO(g)△H1=a kJ/mol 平衡常数K1;
②CO(g)+H2O(g)?H2(g)+CO2(g)△H2=b kJ/mol 平衡常数K2;
③C(s)+H2O(g)?CO(g)+H2(g)△H3 平衡常数K3.
则K1、K2、K3之间的关系是:K3=K1×K2,△H3=(a+b)kJ/mol(用含a、b的代数式表示).
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题.已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下表所示:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(4)在催化剂存在条件下反应:H2O(g)+CO(g)?CO2(g)+H2(g),CO转化率随蒸气添加量的压强比及温度变化关系如图1所示:

对于气相反应,用某组分(B)的平衡分压强(PB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=$\frac{P(C{O}_{2})P({H}_{2})}{P(CO)P({H}_{2}O)}$,提高p[H2O(g)]:p(CO)比,则Kp不变(填“变大”、“变小”或“不变”).实际上,在使用铁镁催化剂的工业流程中,一般采用400℃左右、p[H2O(g)]:p(CO)=3~5.其原因可能是①该温度下催化剂活性最大②该压强比下,反应物转化率已经接近98%.
(5)工业上可利用原电池原理除去工业尾气中的CO并利用其电能,反应装置如图2所示,请写出负极的电极反应式:CO-2e-+CO32-=2CO2.
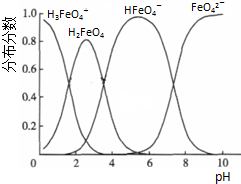
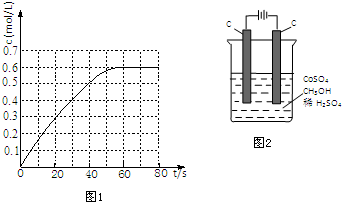
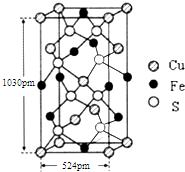 黄血盐(亚铁氰化钾,K4[Fe(CN)6])易溶于水,广泛用作食盐添加剂(抗结剂),食盐中黄血盐的最大使用量为10mg•kg-1.黄血盐经长时间火炒,超过400℃时会分解生成剧毒的氰化钾.回答下列问题:
黄血盐(亚铁氰化钾,K4[Fe(CN)6])易溶于水,广泛用作食盐添加剂(抗结剂),食盐中黄血盐的最大使用量为10mg•kg-1.黄血盐经长时间火炒,超过400℃时会分解生成剧毒的氰化钾.回答下列问题: