9.下列有关叙述正确的是( )
| A. | 加入催化剂会改变反应的焓变 | |
| B. | 已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2,则△H1<△H2 | |
| C. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol | |
| D. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 |
8.A、B、C、D均是短周期元素,其中A、D处于同一周期,B、C处于同一周期,A、D的最低价离子分别为A2-、D-,B+和D-具有相同的电子层结构,元素C的简单离子是同周期元素中半径最小的.下列说法不正确的是( )
| A. | 离子半径:A2->D->B+ | |
| B. | 元素B、C的最高价氧化物对应水化物的碱性:B>C | |
| C. | 简单氢化物的稳定性:A>D | |
| D. | A与B形成的化合物中可能既有离子键又有共价键 |
7.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 7.8g苯中含有的碳碳双键数目为0.3NA | |
| B. | 标准状况下,22.4L Cl2通入足量的石灰乳制备漂白粉,转移电子数为2NA | |
| C. | 常温常压下,17g甲基(-14CH3)中所含的中子数为9NA | |
| D. | 4.6g金属钠与足量O2充分反应后,所得固体中阴、阳离子的总数为0.3NA |
6.下列离子组能大量共存,且加入相应试剂后发生反应的离子方程式正确的是( )
| 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 | |
| A | Fe3+、I-、ClO- | NaOH溶液 | Fe3++3OH-═Fe(OH)3↓ |
| B | Fe2+、NO3-、K+ | 稀硫酸 | 3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| C | Ba2+、HCO3-、Cl- | NaOH溶液 | HCO3-+OH-═CO32-+H2O |
| D | Ag+、F-、NO3- | 过量氨水 | Ag++OH-═AgOH↓ |
| A. | A | B. | B | C. | C | D. | D |
5.Na2S2O3可用作照相的定影剂等.已知Na2S2O3的某些性质如下:
(Ⅰ)S2O32-能被I2氧化为S4O62-;
(Ⅱ)酸性条件下S2O32-迅速分解为S和SO2;
(Ⅲ)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3;所得产品中常含有少量Na2SO3和Na2SO4.
实验室可用如下装置(略去部分夹持仪器)模仿生成过程.
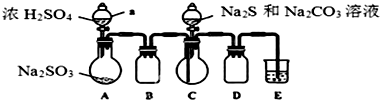
实验步骤:(1)仪器组装完成后,关闭A、C中分液漏斗活塞,将E中导管伸入盛水的水槽中,微热A中圆底烧瓶,E中导管口有气泡冒出,停止加热,导管中回流一段稳定的水柱,则整个装置气密性良好.装置D的作用是防止倒吸,装
置E中溶液的作用是吸收多余的SO2.
(2)先向C中烧瓶加入Na2CO3和Na2S混合溶液,再向A中烧瓶滴加浓H2SO4.
(3)等Na2CO3和Na2S完全消耗后,结束反应.过滤C中混合物,将溶液蒸发、结晶、过滤、洗涤、干燥,得到产品.
(4)为验证产品中含有硫酸盐,该小组设计了以下实验方案,请将方案补充完整.
(5)利用KMnO4标准溶液可以定量测定硫代硫酸钠试剂的纯度,步骤为:
①溶液配制:称取1.0g Na2S2O3试样,用新煮沸并冷却的蒸馏水溶解,最终定容至100mL.
②滴定:取10.00mL0.01mol•L-1KMnO4标准溶液,加硫酸酸化,再加过量KI溶液.写出该反应的离子反应:2MnO4-+16H++10I-═5I2+2Mn2++8H2O
③往步骤②所得溶液加入某指示剂,用Na2S2O3滴定至终点(2S2O32-+I2═S4O62-+2I-),记录Na2S2O3溶液用量,滴定3次.指示剂最好选用淀粉溶液,本次滴定时所用的玻璃仪器除锥形瓶外,还有碱式滴定管.
④若3次滴定NaS2O3溶液的平均用量为12.00mL,则样品的纯度为65.8%.
(Ⅰ)S2O32-能被I2氧化为S4O62-;
(Ⅱ)酸性条件下S2O32-迅速分解为S和SO2;
(Ⅲ)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3;所得产品中常含有少量Na2SO3和Na2SO4.
实验室可用如下装置(略去部分夹持仪器)模仿生成过程.

实验步骤:(1)仪器组装完成后,关闭A、C中分液漏斗活塞,将E中导管伸入盛水的水槽中,微热A中圆底烧瓶,E中导管口有气泡冒出,停止加热,导管中回流一段稳定的水柱,则整个装置气密性良好.装置D的作用是防止倒吸,装
置E中溶液的作用是吸收多余的SO2.
(2)先向C中烧瓶加入Na2CO3和Na2S混合溶液,再向A中烧瓶滴加浓H2SO4.
(3)等Na2CO3和Na2S完全消耗后,结束反应.过滤C中混合物,将溶液蒸发、结晶、过滤、洗涤、干燥,得到产品.
(4)为验证产品中含有硫酸盐,该小组设计了以下实验方案,请将方案补充完整.
| 实验步骤 | 预期现象或结论 |
| 步骤1:取少量固体样品溶于无氧蒸馏水中 | 固体完全溶解得无色澄清溶液 |
| 步骤2:加入过量盐酸 | |
| 步骤3:静置后取上清液,加入BaCl2溶液 |
①溶液配制:称取1.0g Na2S2O3试样,用新煮沸并冷却的蒸馏水溶解,最终定容至100mL.
②滴定:取10.00mL0.01mol•L-1KMnO4标准溶液,加硫酸酸化,再加过量KI溶液.写出该反应的离子反应:2MnO4-+16H++10I-═5I2+2Mn2++8H2O
③往步骤②所得溶液加入某指示剂,用Na2S2O3滴定至终点(2S2O32-+I2═S4O62-+2I-),记录Na2S2O3溶液用量,滴定3次.指示剂最好选用淀粉溶液,本次滴定时所用的玻璃仪器除锥形瓶外,还有碱式滴定管.
④若3次滴定NaS2O3溶液的平均用量为12.00mL,则样品的纯度为65.8%.
4.碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H2(g)+I2(?)═2HI(g);△H=+9.48kJ/mol
②H2(g)+I2(?)═2HI(g);△H=-26.48kJ/mol
下列判断正确的是( )
①H2(g)+I2(?)═2HI(g);△H=+9.48kJ/mol
②H2(g)+I2(?)═2HI(g);△H=-26.48kJ/mol
下列判断正确的是( )
| A. | ①中的I2为固态,②中的I2为气态 | |
| B. | ②的反应物总能量比①的反应物总能量低 | |
| C. | ①的产物比②的产物热稳定性更好 | |
| D. | 1 mol固态碘升华时将吸热17 kJ |
3.常温下浓度均为0.1mol/L的四种盐溶液,其pH如表所示,下列说法正确的是( )
0 152073 152081 152087 152091 152097 152099 152103 152109 152111 152117 152123 152127 152129 152133 152139 152141 152147 152151 152153 152157 152159 152163 152165 152167 152168 152169 152171 152172 152173 152175 152177 152181 152183 152187 152189 152193 152199 152201 152207 152211 152213 152217 152223 152229 152231 152237 152241 152243 152249 152253 152259 152267 203614
| 序号 | ① | ② | ③ | ④ |
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.8 | 9.7 | 11.6 | 10.3 |
| A. | 将等浓度的CH3COOH和HClO溶液,pH小的是HClO | |
| B. | Na2CO3和NaHCO3溶液中粒子种类不同 | |
| C. | 溶液水的电离程度①>②>④>③ | |
| D. | NaHCO3溶液中,c(Na +)=c(CO3 2-)+c(HCO3-)+c(H2CO3) |
 .
.