19.W、X、Y是原子序数依次增大的同一短周期元素.W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y.下列说法不正确的是( )
| A. | 原子半径W>X>Y | B. | W2Y的电子式为: | ||
| C. | 元素的金属性W<X | D. | W2Y2中既有离子键,又有共价键 |
15.Na2O、Na2CO3组成的固体混合物8.0g与质量分数为36.5%的盐酸20.0g恰好反应完全(至不再产生气体),蒸干溶液,最终得到的固体质量为( )
| A. | 8.0g | B. | 11.7g | C. | 23.4g | D. | 无法计算 |
14.下列离子方程式的书写正确的是( )
| A. | Cl2与H2O反应:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Fe与稀硫酸反应:Fe+2H+═Fe3++H2↑ | |
| C. | 氨水与FeCl3溶液反应:3OH-+Fe3+═Fe(OH)3↓ | |
| D. | NaOH与盐酸反应:OH-+H+═H2O |
13.下列说法中,不正确的是( )
| A. | Na2CO3水溶液呈碱性,所以其热溶液可以除去物品表面的油污 | |
| B. | Fe(OH)3胶体能吸附水中的悬浮颗粒并沉降,因而具有杀菌作用 | |
| C. | 钠钾合金可用于快中子反应堆作热交换剂 | |
| D. | 钠的还原性很强,可以用来冶炼锆、钛等贵重金属 |
12.在化学反应 3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+3H2 中,H2O的作用是( )
| A. | 还原剂 | B. | 氧化剂 | C. | 催化剂 | D. | 溶剂 |
11.对于反应N2O4(g)?2NO2(g)在温度一定时,平衡体系中NO2的体积分数(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是( )

| A. | A、C两点的正反应速率的关系为A>C | |
| B. | A、B、C、D、E各状态中,v(正)<v(逆)的是状态E | |
| C. | 维持P1不变,E→A所需时间为x;维持P2不变,D→C所需时间为y,则x<y | |
| D. | 使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是从P1突然加压至P2,再由P2无限缓慢降压至P1 |
10.在某温度时,将nmol/L的氨水滴入10mL0.1mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示.下列有关说法正确的是( )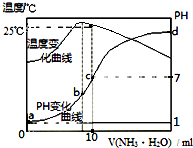
0 152048 152056 152062 152066 152072 152074 152078 152084 152086 152092 152098 152102 152104 152108 152114 152116 152122 152126 152128 152132 152134 152138 152140 152142 152143 152144 152146 152147 152148 152150 152152 152156 152158 152162 152164 152168 152174 152176 152182 152186 152188 152192 152198 152204 152206 152212 152216 152218 152224 152228 152234 152242 203614

| A. | a点KW=1.0×10-14 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | b点:c(NH4+)>c(Cl-)>c(H+)>c(OH-) | |
| D. | 25℃时,一水合氨的电离平衡常数为$\frac{1{0}^{-7}}{(10n-1)}$(用n表示) |
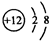 ,S2-的结构示意图
,S2-的结构示意图 .
.