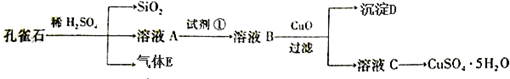
7.关于Na2CO3与NaHCO3说法正确的是( )
| A. | 等质量的两物质分别与足量盐酸充分反应时,NaHCO3产生CO2气体多 | |
| B. | 可以用澄清石灰水或者氢氧化钠溶液区别 | |
| C. | 等质量的两物质分别与足量的等浓度盐酸反应时,一般是Na2CO3产生CO2气体快 | |
| D. | NaHCO3中Na2CO3混有杂质可以用加热方法除去 |
6.下列离子方程式的书写正确的是( )
| A. | 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 钠和冷水反应 Na+2H2O═Na++2OH-+H2↑ | |
| C. | 氢氧化钡溶液与稀 H2SO4 反应:Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O | |
| D. | 少量NaHCO3溶液与Ca(OH)2溶液反应:OH-+HCO3-═CO32-+H2O |
5.在下列变化中,一定需要另外加入氧化剂才能实现的是( )
| A. | HCl→H2 | B. | Br-→Br2 | C. | Fe2O3→Fe | D. | KMnO4→O2 |
4.下列实验能达到预期目的是( )
| A. | 用分液法可分离植物油和水 | |
| B. | 用过滤法可出去食盐中混有的Fe(OH)3胶体 | |
| C. | 用酒精萃取碘水中的碘 | |
| D. | 用盐酸可除去Mg中混有的Al |
3.根据反应:2KClO3+I2═2KIO3+Cl2↑判断,下列结论不正确的是( )
| A. | 该反应属于置换反应 | B. | I2具有还原性 | ||
| C. | 当生成1mol Cl2时转移2mol电子 | D. | 氧化剂是KClO3 |
2.下列溶液中离子一定能大量共存的是( )
| A. | 与铝产生氢气的溶液中:NH4+、Cl-、Mg2+、SO42- | |
| B. | 常温下PH=9的溶液中:Na+、K+、AlO2-、SO42- | |
| C. | 0.1mol/LNaOH溶液中:HCO3-、Na+、K+、Ca2+ | |
| D. | 无色溶液中:H+、Cu2+、Al3+、NO3- |
1.若NA代表阿伏伽德罗常数,则下列有关阿伏伽德罗常数的说法正确的是( )
| A. | 1molNa与足量氧气充分反应转移电子数目为NA | |
| B. | 1L0.1mol/LHCl溶液中含0.1NAHCl分子 | |
| C. | 100ml 1mol/L盐酸与0.1molNa2CO3无论如何滴加都产生0.05NA的CO2分子 | |
| D. | 0.1mol/L的AlCl3中Cl-的物质的量为0.3NA |
20.下列有关物质应用说法错误的是( )
| A. | 小苏打可以做发酵粉 | |
| B. | 过氧化钠可用于呼吸面具或潜水艇中作为供氧剂 | |
| C. | 铁红常用作红色油漆或涂料 | |
| D. | 钠可以从硫酸铜溶液中置换出铜 |
19.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理.某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如图.
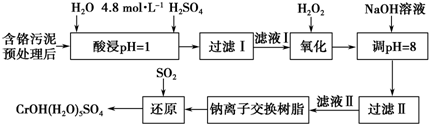
其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.
(1)实验室用98%(密度是1.84g/cm3)的浓硫酸配制250mL 4.8mol•L-1的H2SO4溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需250mL容量瓶、胶头滴管,需要取用65.2ml98%(密度是1.84g/cm3)的浓硫酸.
(2)酸浸时,为了提高浸取率可采取的措施有升高反应温度;增大固体颗粒的表面积(答出两点).
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:2Cr3++3H2O2+H2O=Cr2O72-+8H+.
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如表:
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-.滤液Ⅱ中阳离子主要有Na+、Mg2+、Ca2+;但溶液的pH不能超过8,其理由是pH超过8会使部分Al(OH)3溶解生成AlO2-,最终影响Cr(III)回收与再利用.
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液Ⅱ中的金属阳离子是Ca2+、Mg2+.
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.
0 152021 152029 152035 152039 152045 152047 152051 152057 152059 152065 152071 152075 152077 152081 152087 152089 152095 152099 152101 152105 152107 152111 152113 152115 152116 152117 152119 152120 152121 152123 152125 152129 152131 152135 152137 152141 152147 152149 152155 152159 152161 152165 152171 152177 152179 152185 152189 152191 152197 152201 152207 152215 203614

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+.
(1)实验室用98%(密度是1.84g/cm3)的浓硫酸配制250mL 4.8mol•L-1的H2SO4溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需250mL容量瓶、胶头滴管,需要取用65.2ml98%(密度是1.84g/cm3)的浓硫酸.
(2)酸浸时,为了提高浸取率可采取的措施有升高反应温度;增大固体颗粒的表面积(答出两点).
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:2Cr3++3H2O2+H2O=Cr2O72-+8H+.
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如表:
| 阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | - | - | - |
| 沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
(5)钠离子交换树脂的反应原理为Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去的滤液Ⅱ中的金属阳离子是Ca2+、Mg2+.
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:3SO2+2Na2CrO4+12H2O=2CrOH(H2O)5SO4↓+Na2SO4+2NaOH.