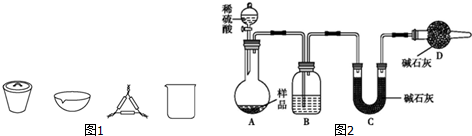
7.反应H2(g)+Br2(g)?2HBr(g)△H<0,达平衡后,其他条件不变,温度从773K突变到573K时,化学平衡常数K与$\frac{{c}^{2}(HBr)}{c({H}_{2})•c(B{r}_{2})}$的关系和平衡移动的方向都正确的是( )
| A. | K>$\frac{{c}^{2}(HBr)}{c({H}_{2})•c(B{r}_{2})}$,平衡向正反应方向移动 | |
| B. | K>$\frac{{c}^{2}(HBr)}{c({H}_{2})•c(B{r}_{2})}$,平衡向逆反应方向移动 | |
| C. | K<$\frac{{c}^{2}(HBr)}{c({H}_{2})•c(B{r}_{2})}$,平衡向正反应方向移动 | |
| D. | K<$\frac{{c}^{2}(HBr)}{c({H}_{2})•c(B{r}_{2})}$,平衡向逆反应方向移动 |
6.反应A(g)+3B(g)?2C(g)△H<0,达平衡后,将反应体系的温度升高,下列叙述中正确的是( )
| A. | 逆反应速率增大更大,平衡向逆反应方向移动 | |
| B. | 正反应速率增大更大,平衡向正反应方向移动 | |
| C. | 正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 | |
| D. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
5.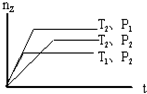 反应 2X(g)+Y(g)?2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )
反应 2X(g)+Y(g)?2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )
 反应 2X(g)+Y(g)?2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )
反应 2X(g)+Y(g)?2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示.下列判断正确的是( )| A. | T1<T2,P1<P2,△H<0 | B. | T1<T2,P1>P2,△H>0 | ||
| C. | T1>T2,P1>P2,△H<0 | D. | T1>T2,P1<P2,△H>0 |
3.将0.2mol•L-1HA溶液和0.1mol•L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的( )
| A. | c(HA)<c(A-) | B. | c(Na+)=c(A-)+c(HA) | ||
| C. | c(HA)-c(A-)=c(OH-) | D. | c(HA)+c(A-)=0.1mol/L |
2.下列离子方程式的表达正确的是( )
| A. | 金属铝溶于氢氧化钠溶液:Al+2OH-═2AlO2-+H2↑ | |
| B. | NaHCO3溶液与硫酸氢钠溶液混合:HCO3-+H+═H2O+CO2↑ | |
| C. | 过氧化钠与水反应:Na2O2+2H2O═2Na++2OH-+O2↑ | |
| D. | Ca(OH)2溶液中通入过量CO2:Ca2++2OH-+CO2═CaCO3↓+H2O |
20.短周期元素甲、乙、丙、丁的原子半径依次增大,其氢化物中甲、乙、丙、丁的化合价如表所示.下列说法中正确的是( )
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 化合价 | -2 | -3 | -4 | -3 |
| A. | 含氧酸的酸性:乙<丁 | B. | 元素非金属性:甲<乙 | ||
| C. | 丙所形成的单质可能互为同位素 | D. | 氢化物的沸点:甲>丁 |
19.用0.10mol•L-1的盐酸滴定0.10mol•L-1的氨水,滴定过程中不可能出现的结果是( )
0 151986 151994 152000 152004 152010 152012 152016 152022 152024 152030 152036 152040 152042 152046 152052 152054 152060 152064 152066 152070 152072 152076 152078 152080 152081 152082 152084 152085 152086 152088 152090 152094 152096 152100 152102 152106 152112 152114 152120 152124 152126 152130 152136 152142 152144 152150 152154 152156 152162 152166 152172 152180 203614
| A. | c(NH4+)>c(Cl-),c(OH-)>c(H+) | B. | c(Cl-)>c(NH4+),c(OH-)>c(H+) | ||
| C. | c(Cl-)>c(NH4+),c(H+)>c(OH-) | D. | c(NH4+)=c(Cl-),c(OH-)=c(H+) |