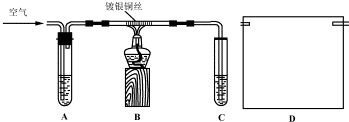
19.下列实验操作都能够达到预期目的是( )
①用pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
①用pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
| A. | ②④⑥ | B. | ②⑥ | C. | ⑤ | D. | ④⑤⑥ |
14.医学研究证明,用放射性$\stackrel{135}{53}$I治疗肿瘤可收到一定疗效,下列有关$\stackrel{135}{53}$I叙述正确的是( )
| A. | $\stackrel{135}{53}$I是碘的一种同素异形体 | |
| B. | $\stackrel{135}{53}$I是一种新发现的元素 | |
| C. | $\stackrel{135}{53}$I位于元素周期表中第四周期ⅦA族 | |
| D. | $\stackrel{135}{53}$I核内的中子数与核外电子数之差为29 |
13.(Ⅰ)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇. 某化学研究性学习小组模拟工业合成甲醇的反应(△H<0),在容积固定为2L的密闭容器内充入1molCO和 2molH2,加入合适催化剂(体积可以忽略不计)后在250°C开始反应,并用压力计监测容器内压强的变化如下:
(1)从反应开始到20min时,以CO表示的平均反应速率=0.0125mol/(L•min),
(2)该温度下平衡常数K=4(mol/L)-2,,若升高温度则K值减小(填“增大”、“减小”或“不变”);
(3)下列描述中能说明上述反应已达平衡的是BC;
A.2v (H2)正=v (CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成 n molCO 的同时生成 2n molH2
(Ⅱ)在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:
2SO2(g)+O2(g)?2SO3(g)△H=-190kJ•mol-1
(1)该反应500℃时的平衡常数<450℃时的平衡常数(填“>”、“<”或“=”).
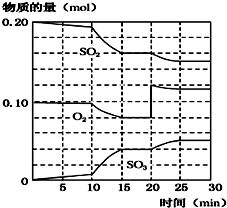
(2)450℃时,在一2L密闭容器中,将二氧化硫和氧化混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是15~20 min和25~30 min.
(3)据图判断,反应进行至20min时,曲线发生变化的原因是增大O2浓度(通入O2);(用文字表达),10min到15min的曲线变化的原因可能是AB(填字母).
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加SO3物质的量
(4)欲提高SO2的转化率,下列措施可行的是b.(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度.
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
(2)该温度下平衡常数K=4(mol/L)-2,,若升高温度则K值减小(填“增大”、“减小”或“不变”);
(3)下列描述中能说明上述反应已达平衡的是BC;
A.2v (H2)正=v (CH3OH)逆
B.容器内气体的平均摩尔质量保持不变
C.容器中气体的压强保持不变
D.单位时间内生成 n molCO 的同时生成 2n molH2
(Ⅱ)在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:

2SO2(g)+O2(g)?2SO3(g)△H=-190kJ•mol-1
(1)该反应500℃时的平衡常数<450℃时的平衡常数(填“>”、“<”或“=”).
(2)450℃时,在一2L密闭容器中,将二氧化硫和氧化混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是15~20 min和25~30 min.
(3)据图判断,反应进行至20min时,曲线发生变化的原因是增大O2浓度(通入O2);(用文字表达),10min到15min的曲线变化的原因可能是AB(填字母).
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加SO3物质的量
(4)欲提高SO2的转化率,下列措施可行的是b.(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度.
12.如表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下列化合物与氯化氢加成时,取代基对速率的影响与表中规律类似,其中反应速率最快的是A(填序号).
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
CH2=CHCH2CH3+H2O$\stackrel{H+}{→}$CH3CH(OH)CH2CH3+CH3CH2CH2CH2OH
(主要产物) (次要产物)
请写出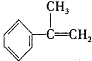 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式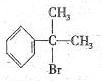 .
.
(3)禽流感在全球的蔓延,使人们谈“禽”色变.从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物.
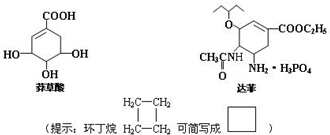
a.莽草酸分子中含有的官能团有羧基、羟基、碳碳双键;
b.莽草酸在浓硫酸作用下加热可以得到B(B的结构简式为: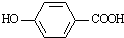 ),其反应类型为:消去反应;
),其反应类型为:消去反应;
c.请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):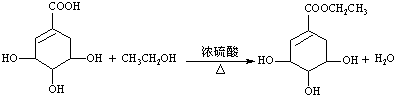 .
.
0 151957 151965 151971 151975 151981 151983 151987 151993 151995 152001 152007 152011 152013 152017 152023 152025 152031 152035 152037 152041 152043 152047 152049 152051 152052 152053 152055 152056 152057 152059 152061 152065 152067 152071 152073 152077 152083 152085 152091 152095 152097 152101 152107 152113 152115 152121 152125 152127 152133 152137 152143 152151 203614
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3
C.CH2=CH CH3 D.CH2=CHCl
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3+HBr→CH3CHBrCH3+CH3CH2Br
(主要产物)(次要产物)
CH2=CHCH2CH3+H2O$\stackrel{H+}{→}$CH3CH(OH)CH2CH3+CH3CH2CH2CH2OH
(主要产物) (次要产物)
请写出
 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式 .
.(3)禽流感在全球的蔓延,使人们谈“禽”色变.从香料八角中提取的莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一,达菲是抗禽流感病毒特效药物.

a.莽草酸分子中含有的官能团有羧基、羟基、碳碳双键;
b.莽草酸在浓硫酸作用下加热可以得到B(B的结构简式为:
 ),其反应类型为:消去反应;
),其反应类型为:消去反应;c.请写出莽草酸与乙醇反应的化学方程式(有机物用结构简式表示):
 .
. 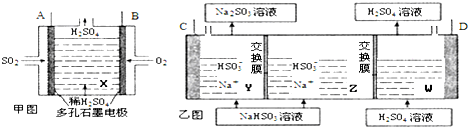
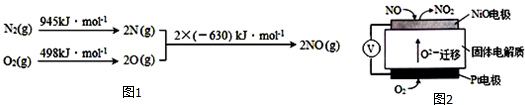
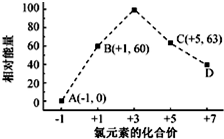 元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.
元素周期表中第 VIIA族元素的单质及其化合物的用途广泛.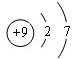 .
.