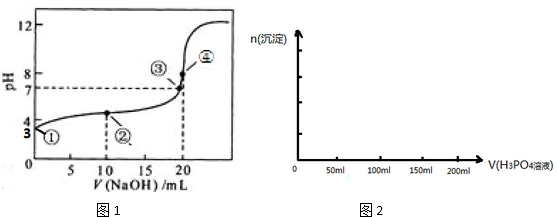
4.(1)常温下,用 0.1000mol•L-1NaOH溶液滴定 20.00mL 0.1000mol•L-1CH3COOH溶液所得滴定曲线如图1.已知起始①点溶液的pH为3,③点溶液的pH为7,则Ka(CH3COOH)=10-5
(2)在用Na2SO3溶液吸收SO2过程中,pH随n(SO32-):n(HSO32-)变化关系如下表:
0.01mol•L-1 Na2SO3溶液中通入SO2至溶液呈中性时,溶液中的所有离子的浓度由大到小的顺序是c(Na+)>c(HSO3-)>c(SO32-)>c(H+)=c(OH-)
(3)向0.1mol•L的NaHSO3中通入氨气至溶液呈中性时,溶液中的c(H+)、c(OH-)、c(SO32-)、c(Na+)、c(NH4+)这五种离子浓度大小关系是c(Na+)>c(SO32-)>c(NH4+)>c(H+)=c(OH-)
(4)已知Ca3(PO4)2、CaHPO4均难溶于水,而Ca(H2PO4)2易溶,在含0.1mol Ca(OH)2的澄清石灰水中逐渐加入1mol•L-1的H3PO4;请作出生成沉淀的物质的量随H3PO4滴入体积从0开始至200mL的图象.

(2)在用Na2SO3溶液吸收SO2过程中,pH随n(SO32-):n(HSO32-)变化关系如下表:
| n(SO32-):n(HSO3-) | 1:9 | 1:1 | 1:91 |
| pH | 8.2 | 7.2 | 6.2 |
(3)向0.1mol•L的NaHSO3中通入氨气至溶液呈中性时,溶液中的c(H+)、c(OH-)、c(SO32-)、c(Na+)、c(NH4+)这五种离子浓度大小关系是c(Na+)>c(SO32-)>c(NH4+)>c(H+)=c(OH-)
(4)已知Ca3(PO4)2、CaHPO4均难溶于水,而Ca(H2PO4)2易溶,在含0.1mol Ca(OH)2的澄清石灰水中逐渐加入1mol•L-1的H3PO4;请作出生成沉淀的物质的量随H3PO4滴入体积从0开始至200mL的图象.
2.下列叙述错误的是( )
| A. | 中和同体积同浓度的HAc和HCl,所需碱的物质的量是相同的 | |
| B. | 由H2CO3的解离平衡,可知溶液中[H+]和[CO32-]的比值=2:1 | |
| C. | 某弱酸溶液越稀,其电离度越大 | |
| D. | 强电解质溶液无离解常数,但可以有溶度积常数 |
1.如果将20mL 12mol•L-1的浓盐酸与足量KMnO4充分反应,实际能收集到的氯气在标准状况下的体积将( )
| A. | ≥1.68L | B. | >1.68L | C. | ≤1.68L | D. | <1.68L |
19.在2L密闭容器内,按物质的量之比为2:1投入NO和O2.某温度下发生如下反应:2NO(g)+O2(g)═2NO2(g),n(NO)随时间的变化如表:
下列说法不正确的是( )
0 151943 151951 151957 151961 151967 151969 151973 151979 151981 151987 151993 151997 151999 152003 152009 152011 152017 152021 152023 152027 152029 152033 152035 152037 152038 152039 152041 152042 152043 152045 152047 152051 152053 152057 152059 152063 152069 152071 152077 152081 152083 152087 152093 152099 152101 152107 152111 152113 152119 152123 152129 152137 203614
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.015 | 0.012 | 0.010 | 0.010 | 0.010 |
| A. | 在0~2s内,v(O2)=0.002mol•L-1•s-1 | |
| B. | 5s后向容器中通入0.02mol NO2,再次平衡后,0.020mol<n(NO2)<0.040 mol | |
| C. | 在该温度时,向容器中加入O2,平衡将正向移动,平衡常数增大 | |
| D. | 5s后,向反应容器中同时通入各0.01mol的NO、O2、NO2,平衡向正向移动 |

 已知25℃时,氢氟酸(HF)的电离平衡常数K=3.6×10-4,氢氰酸(HCN)的电离平衡常数K=4.9×10-10
已知25℃时,氢氟酸(HF)的电离平衡常数K=3.6×10-4,氢氰酸(HCN)的电离平衡常数K=4.9×10-10 A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C
