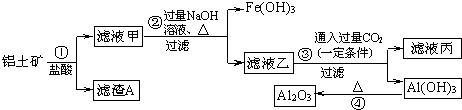
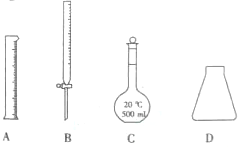
18.下列性质不属于金属共性的是( )
| A. | 电热的良导体 | B. | 金属阳离子的氧化性 | ||
| C. | 单质的还原性 | D. | 高沸点 |
16.下列说法正确的是( )
| A. | Na2O2、MgO、Fe2O3均属碱性氧化物 | |
| B. | NaHCO3、NaAlO2、Na2CO3均属钠盐 | |
| C. | Al(OH)3、Fe(SCN)3、BaSO4均属难电离物质 | |
| D. | Al(OH)3、Fe(OH)3、Fe(OH)2均属碱 |
15.下列化合物在加热时不能与新制Cu(OH)2反应的是( )
| A. | CH3CHO | B. | CH3CH2OH | C. | HCOOH |
14.下列化合物中不能使酸性高锰酸钾溶液褪色的是( )
| A. | 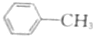 | B. | CH2═CHCH2OH | C. | 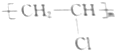 |
13.有关物质结构的下列说法中正确的是( )
| A. | 石油裂解只破坏极性键 | |
| B. | 含极性键的共价化合物一定是电解质 | |
| C. | 氯化钠固体中的离子键在溶于水时被破坏 | |
| D. | HF的分子间作用力大于HCl,故HF比HCl稳定 |
11.禁止用工业酒精配置饮料,是因为工业酒精中含有某种毒性很强的醇,该醇是( )
| A. | 甲醇 | B. | 乙二醇 | C. | 丙三醇 | D. | 异戊醇 |
10.下列给出几种物质的熔点数据:
回答下列问题:
(1)推测以下几种物质的晶体类型:MgO离子晶体,AlCl3分子晶体,晶体B原子晶体,CCl4分子晶体.
(2)推测晶格能大小:NaCl的晶格能大于(填“大于”或“小于”)KCl的晶格能.经测定NaCl晶体中离子间距为276pm,MgO晶体中离子间距为205pm,MgO的熔点比NaCl的高出很多,其主要原因是电荷数多,晶格能大.
(3)CBr4分子的空间构型是正四面体,导致CBr4的熔点大于CCl4熔点的主要原因是CBr4的相对分子质量大于CCl4的相对分子质量,所以CBr4的熔点大于CCl4熔点.
0 151872 151880 151886 151890 151896 151898 151902 151908 151910 151916 151922 151926 151928 151932 151938 151940 151946 151950 151952 151956 151958 151962 151964 151966 151967 151968 151970 151971 151972 151974 151976 151980 151982 151986 151988 151992 151998 152000 152006 152010 152012 152016 152022 152028 152030 152036 152040 152042 152048 152052 152058 152066 203614
| NaCl | KCl | MgO | AlCl3 | SiC | 晶体B | CCl4 | CBr | |
| 熔点/℃ | 801 | 772 | 2800 | 190 | 2600 | 2300 | -22.9 | 90 |
(1)推测以下几种物质的晶体类型:MgO离子晶体,AlCl3分子晶体,晶体B原子晶体,CCl4分子晶体.
(2)推测晶格能大小:NaCl的晶格能大于(填“大于”或“小于”)KCl的晶格能.经测定NaCl晶体中离子间距为276pm,MgO晶体中离子间距为205pm,MgO的熔点比NaCl的高出很多,其主要原因是电荷数多,晶格能大.
(3)CBr4分子的空间构型是正四面体,导致CBr4的熔点大于CCl4熔点的主要原因是CBr4的相对分子质量大于CCl4的相对分子质量,所以CBr4的熔点大于CCl4熔点.