8.电解水﹙H2O﹚和重水﹙D2O﹚的混合物,通电一定时间后,两极共生成气体18.5克,体积为33,6L﹙标况﹚,所生成的气体中重氢﹙D﹚和普氢﹙H﹚的原子个数比是( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
7.下列事实不属于盐类水解应用的是( )
| A. | 明矾、氯化铁晶体常用于净水 | |
| B. | 实验室制氢气时加CuSO4可加快反应速率 | |
| C. | 实验室配制FeCl3溶液时加入少量稀盐酸 | |
| D. | 实验室通常使用热的纯碱溶液去除油污 |
6.在298K、1.01×105 Pa下,将22gCO2通入750mL 1mol•L-1 NaOH 溶液中充分反应,测得反应放出x kJ的热量.已知在该条件下,1molCO2通入1L2mol•L-1 NaOH溶液中充分反应放出y kJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x) kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| D. | CO2(g)+2NaOH(l)═2NaHCO3(l)△H=-(8x-2y) kJ•mol-1 |
4.根据反应(1)~(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是( )
(1)Cl2+2KI=2KCl+I2
(2)2FeCl2+Cl2=2FeCl3
(3)2FeCl3+2HI=2FeCl2+2HCl+I2
(4)H2S+I2=S+2HI.
(1)Cl2+2KI=2KCl+I2
(2)2FeCl2+Cl2=2FeCl3
(3)2FeCl3+2HI=2FeCl2+2HCl+I2
(4)H2S+I2=S+2HI.
| A. | H2S>I2>Fe3+>Cl2 | B. | Cl2>Fe3+>I2>H2S | ||
| C. | Fe3+>Cl2>H2S>I2. | D. | Cl2>I2>Fe3+>H2S |
2.下列各图示中能较长时间看到Fe(OH)2白色沉淀的是( )
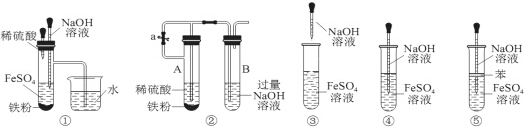

| A. | ①②③④⑤ | B. | ①②⑤ | C. | ①②③④ | D. | ②④⑤ |
1.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.下列说法正确的是( )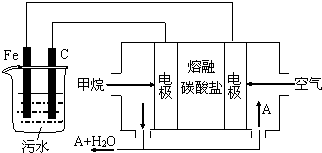

| A. | 该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,则负极的电极反应是CH4+4CO32--8e-═5CO2+2H2O | |
| B. | 实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣,此时,可以向污水中加入适量的稀H2SO4 | |
| C. | 实验过程中,若阴极产生2mol气体,则燃料电池消耗11.2L CH4 | |
| D. | 为了使该电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A参加循环,则A物质是CO32- |
20.Cl2O为国际公认高效安全灭菌消毒剂之一,它是棕黄色强刺激性气体,沸点3.8℃,熔点-116℃.实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,装置如下(图Ⅰ):
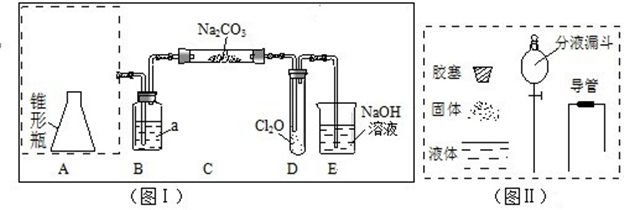
回答下列问题:
(1)把浓盐酸直接滴在KMnO4晶体上就可以产生Cl2.请模仿“图Ⅱ”在“图Ⅰ”A处补画出正确的装置图,并作必要的标注
(2)B中试剂a应选用b(填下列序号字母):
a.CCl4 b.饱和NaCl溶液 c.浓H2SO4d.饱和NaHCO3溶液
(3)通入适量的氯气,在C中生成黄绿色的物质Cl2O,该物质常温为气体,方程式为:
2Cl2+2Na2CO3+H2O═2NaHCO3+2NaCl+1Cl2O
(4)对C中反应后的固体成分进行检验,请写出实验步骤以及预期的现象和结论.
限选实验试剂和仪器:蒸馏水、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、澄清石灰水、试管、小烧杯、带导管的橡皮塞、过滤装置.
0 151861 151869 151875 151879 151885 151887 151891 151897 151899 151905 151911 151915 151917 151921 151927 151929 151935 151939 151941 151945 151947 151951 151953 151955 151956 151957 151959 151960 151961 151963 151965 151969 151971 151975 151977 151981 151987 151989 151995 151999 152001 152005 152011 152017 152019 152025 152029 152031 152037 152041 152047 152055 203614

回答下列问题:
(1)把浓盐酸直接滴在KMnO4晶体上就可以产生Cl2.请模仿“图Ⅱ”在“图Ⅰ”A处补画出正确的装置图,并作必要的标注
(2)B中试剂a应选用b(填下列序号字母):
a.CCl4 b.饱和NaCl溶液 c.浓H2SO4d.饱和NaHCO3溶液
(3)通入适量的氯气,在C中生成黄绿色的物质Cl2O,该物质常温为气体,方程式为:
2Cl2+2Na2CO3+H2O═2NaHCO3+2NaCl+1Cl2O
(4)对C中反应后的固体成分进行检验,请写出实验步骤以及预期的现象和结论.
限选实验试剂和仪器:蒸馏水、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、澄清石灰水、试管、小烧杯、带导管的橡皮塞、过滤装置.
| 实验步骤 | 现象和结论 |
| 步骤一:取C中的少量固体样品于试管中,滴加足量蒸馏水至完全溶解,然后将溶液分别置于a、b试管中. | |
| 步骤二:向a试管中滴加BaCl2溶液,静置. | 无明显现象,证明固体中不含Na2CO3 |
| 步骤三:取a试管的上层清液于c试管中取a试管的上层清液于c试管中加入适量氢氧化钡溶液 | 产生白色沉淀证明固体中含有碳酸氢钠 |
| 步骤四:向试管b中加入过量稀硝酸溶液向试管b中加入过量稀硝酸溶液再滴加少量硝酸银溶液 | 有白色沉淀生成 则证明固体中含有NaCl |
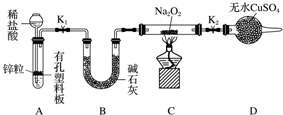 Na2O2可用作漂白剂和呼吸面具中的供氧剂.
Na2O2可用作漂白剂和呼吸面具中的供氧剂.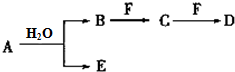 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题: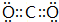 ;D中所含化学键的类型离子键和共价键.
;D中所含化学键的类型离子键和共价键.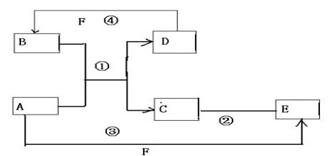
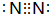 反应?①的化学方程式2NH3+3Cl2=N2+6HCl
反应?①的化学方程式2NH3+3Cl2=N2+6HCl