5.在4L的密闭容器中充入6mol A气体和5mol B气体,在一定条件下发生如下反应:3A(g)+B(g)?2C(g)+xD(g).若经10s后测得生成2molC,D的浓度为0.5mol•L-1,下列几种说法正确的是( )
| A. | x=1 | |
| B. | B的转化率为20% | |
| C. | 反应的10s内A的反应速率为0.3mol•L-1•s-1 | |
| D. | 反应进行到10s时,在相同温度下容器内混合气体的压强是反应前的85% |
13.在和铝反应能生成氢气的无色溶液中,下列各组离子可能大量共存的是( )
| A. | Cl-、Na+、NO3-、Ba2+ | B. | NH4+、HCO3-、Cl-、K+ | ||
| C. | K+、Ba2+、Cl-、SO42- | D. | Cu2+、NH4+、I-、Cl- |
12.下列离子方程式书写正确的是( )
0 151847 151855 151861 151865 151871 151873 151877 151883 151885 151891 151897 151901 151903 151907 151913 151915 151921 151925 151927 151931 151933 151937 151939 151941 151942 151943 151945 151946 151947 151949 151951 151955 151957 151961 151963 151967 151973 151975 151981 151985 151987 151991 151997 152003 152005 152011 152015 152017 152023 152027 152033 152041 203614
| A. | 硫酸铝中加入过量的氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 氢氧化铝与盐酸反应:2Al(OH)3+6H+═2Al3++6H20 | |
| C. | 硫酸铜与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 偏铝酸钠溶液与适量稀硝酸反应:AlO2-+H++H20═Al(OH)3↓ |
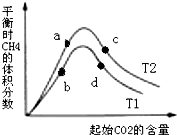 有科学家提出“绿色自由”的构想:将CO2变为燃料或有机化学品.其构想分成3个步骤:
有科学家提出“绿色自由”的构想:将CO2变为燃料或有机化学品.其构想分成3个步骤: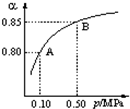 t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),120s时反应达到化学平衡,此时测得反应物O2还剩余0.2mol,请填写下列空白:
t℃时,将2molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g)?2SO3(g),120s时反应达到化学平衡,此时测得反应物O2还剩余0.2mol,请填写下列空白: