9.汽车排放的尾气中含有NO2,NO2是城市大气污染的主要污染物之一.在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染.反应过程为①2NO2-→2NO+2O;②2NO+O2- →2NO2;③O+O2- →O3.下列对该反应过程及产物叙述正确的是( )
| A. | NO2只起还原剂作用 | B. | NO2起催化剂作用 | ||
| C. | NO2只起氧化剂作用 | D. | O3与O2互为同分异构体 |
8.下列反应中的氨与反应4NH3+5O2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$4NO+6H2O中的氨作用相同的是( )
| A. | 2Na+2NH3=2NaNH2+H2↑ | B. | NH3+HCl=NH4Cl | ||
| C. | 4NH3+6NO=5N2+6H2O. | D. | 3SiH4+4NH3=Si3N4+12H2 |
7.某溶液能溶解Al(OH)3,则此溶液中一定能大量共存的离子组是( )
| A. | Mg2+、Cl-、Na+、NO3- | B. | K+、Na+、NO3-、HCO3- | ||
| C. | Na+、K+、Cl-、NO3- | D. | Na+、Cl-、AlO2-、SO42- |
6.某溶液中只含有Na+、Fe3+、Cl-、SO42-四种离子,已知Na+、Fe3+、Cl-的个数比为1:2:3,则溶液中Fe3+和SO42-的个数比为( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
5.在pH=0的无色溶液中能大量共存的离子组是( )
| A. | Na+、Ca2+、Cl-、AlO2- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | Al3+、Cu2+、SO42-、Cl- | D. | NH4+.、Mg2+、SO42-、Cl- |
2. T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表.
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表.
(1)TY2是一种常用的溶剂,是非极性分子(填极性分子或非极性分子),分子中存在2个σ 键.W的最简单氢化物容易液化,理由是氟化氢分子之间存在着氢键.
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号M,该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的第一电离能由大到小顺序为F>O>S(用元素符号作答).
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g/cm3,则晶胞边长为3.61×10-8cm;ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3杂.元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂B.HO2是氧化产物
C.HO2在碱中能稳定存在
D.1mol Z参加反应有1mol电子发生转移.
0 151830 151838 151844 151848 151854 151856 151860 151866 151868 151874 151880 151884 151886 151890 151896 151898 151904 151908 151910 151914 151916 151920 151922 151924 151925 151926 151928 151929 151930 151932 151934 151938 151940 151944 151946 151950 151956 151958 151964 151968 151970 151974 151980 151986 151988 151994 151998 152000 152006 152010 152016 152024 203614
 T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表.
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表.| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/molkJ/mol,I4=11575kJ/mol |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 Ni |
(2)在25℃、101kpa下,已知13.5g的X固体单质在O2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号M,该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的第一电离能由大到小顺序为F>O>S(用元素符号作答).
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g/cm3,则晶胞边长为3.61×10-8cm;ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3杂.元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂B.HO2是氧化产物
C.HO2在碱中能稳定存在
D.1mol Z参加反应有1mol电子发生转移.
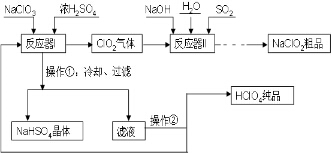 工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下:
工业上生产高氯酸(沸点:90°C)时还同时生产了亚氯酸钠,其工艺流程如下: 现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.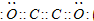 .
.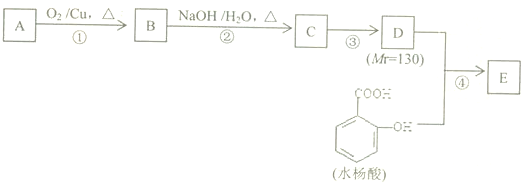
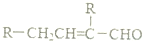
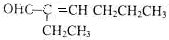 ,若要检验C中所含官能团,一次取样检验,按使用的先后顺序写出所用试剂用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键.
,若要检验C中所含官能团,一次取样检验,按使用的先后顺序写出所用试剂用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键. .
.