1.在Na2SO4 和K2SO4 的混合溶液中,如果c(Na+)=0.2mol/L,c(SO42-)=x mol/L,c(K+)=y mol/L,则x和y的关系是( )
| A. | x=0.5y | B. | x=0.1+0.5y | C. | y=2(x-0.1) | D. | y=2x-0.1 |
20.用石墨电极电解CuSO4溶液一段时间后,向所得溶液中加入0.2mol Cu(OH)2后,恰好使溶液恢复到电解前的浓度.则电解过程中转移的电子的物质的量为( )
| A. | 0.4 mol | B. | 0.5 mol | C. | 0.6 mol | D. | 0.8 mol |
19.金属钠分别与下列物质的溶液反应时,既有气体放出又有白色沉淀生成的是( )
| A. | 盐酸 | B. | 氯化钠 | C. | 氯化铜 | D. | 氯化镁 |
18.对于3Cl2+6NaOH═5NaCl+NaClO3+3H2O的反应,下列说法中不正确的是( )
| A. | Cl2是氧化剂,NaOH是还原剂 | |
| B. | 被氧化的氯原子个数与被还原的氯原子个数比是1:5 | |
| C. | Cl2既是氧化剂,又是还原剂 | |
| D. | 得电子的氯原子个数与失电子的氯原子个数之比为5:1 |
17.已知草酸镍晶体(NiC2O4•2H2O)难溶于水,工业上从废镍催化剂(成分主 要是Ni,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
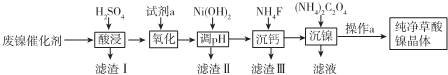
已知:①相关金属离子生成氢氧化物沉淀的pH如表:
②Ksp(CaF2)=1.46×10-10
③当某物质模拟高度小于1.0×10-5mol.L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)pH的调控范围为5.0~6.8,试用化学反应原理的相关知识解释滤渣Ⅱ的生成.5.6~6.8
(4)写出“沉镍”时反应的离子方程式Ni2++C2O42-+2H2O=NiC2O4•2H2O,证明Ni2+已经沉淀完全的实验步骤及现象是取上层清液,继续滴加(NH4)2C2O4溶液,无沉淀生成,
(5)操作a的内容为过滤、洗涤、干燥.

已知:①相关金属离子生成氢氧化物沉淀的pH如表:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
③当某物质模拟高度小于1.0×10-5mol.L-1时,视为完全沉淀.
(1)请写出一种能提高酸浸速率的措施把废镍催化剂粉碎或适当加热、适当增大硫酸浓度、搅拌等.
(2)试剂a是一种绿色氧化剂,写出“氧化”时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)pH的调控范围为5.0~6.8,试用化学反应原理的相关知识解释滤渣Ⅱ的生成.5.6~6.8
(4)写出“沉镍”时反应的离子方程式Ni2++C2O42-+2H2O=NiC2O4•2H2O,证明Ni2+已经沉淀完全的实验步骤及现象是取上层清液,继续滴加(NH4)2C2O4溶液,无沉淀生成,
(5)操作a的内容为过滤、洗涤、干燥.
16.大气中的SO2是造成酸雨的主要污染物.最新研究表明,离子晶体[N(CH3)4]2SO4(s) 能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂:
[N(CH3)4]2SO4(s)+SO2(g)?[N(CH3)4]2S2O6(s)
下列说法正确的是( )
[N(CH3)4]2SO4(s)+SO2(g)?[N(CH3)4]2S2O6(s)
下列说法正确的是( )
| A. | [N(CH3)4]+中只含共价键 | B. | 该反应中,SO2作氧化剂 | ||
| C. | SO2漂白品红是利用其强氧化性 |
15.如图所示的实验,发现烧杯中酸性KMn04溶液褪色.若将烧杯中的溶液换成含有少量KSCN的FeS04溶液,溶液呈血红色.判断下列说法中不正确的是( )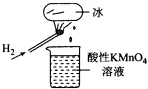

| A. | 该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 | |
| B. | 该条件下H2燃烧的产物中可能含有一定量的H2O2、HO2等 | |
| C. | 将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性 | |
| D. | 酸性FeSO4溶液中加入双氧水的离子反应为:2Fe 2++H2O2+2H+=2Fe3++2H20 |
14.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8 g O2含有5NA个电子 | |
| B. | 1 L 1.0 mol•L-1NaAlO2溶液中含有氧原子数为2NA | |
| C. | 标准状况下,2.24 L CCl4中含有的分子数为0.1NA | |
| D. | 精炼铜的过程中,当阴极析出32 g铜时转移的电子数为NA |
13.下列说法中正确的是( )
0 151823 151831 151837 151841 151847 151849 151853 151859 151861 151867 151873 151877 151879 151883 151889 151891 151897 151901 151903 151907 151909 151913 151915 151917 151918 151919 151921 151922 151923 151925 151927 151931 151933 151937 151939 151943 151949 151951 151957 151961 151963 151967 151973 151979 151981 151987 151991 151993 151999 152003 152009 152017 203614
| A. | 含1 mol Na2CO3的溶液中有Na+的个数为NA | |
| B. | 标准状况下,1 mol任何物质体积均为22.4L | |
| C. | CH4的摩尔质量为16g | |
| D. | 3.01×1023个SO2分子的质量为32g |