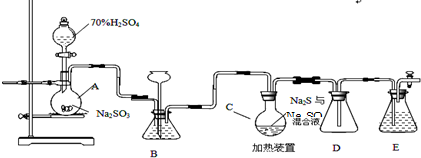
14.下列物质能够导电且属于电解质的是( )
①熔融的氯化钠
②硝酸钾溶液
③硫酸铜晶体
④无水乙醇.
①熔融的氯化钠
②硝酸钾溶液
③硫酸铜晶体
④无水乙醇.
| A. | ① | B. | ①② | C. | ①②③ | D. | ④ |
11.四种常见元素的性质或结构信息如表所示,请问答下列问题.
(1)R的基态原子价层电子排布式为3d104s1,A、B、D这三种元素的第一电离能由大到小的顺序为N>C>Si(写元素符号).
(2)A、B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为NH3,任意写出一种中心原子存在sp2、sp3两种杂化类型的物质的结构简式CH2=CH-CH3,与A的常见单质互为等电子体的上述元素的氧化物是CO.
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中σ键之比为2:1,已知有下列两种数据:
两种氧化物熔点、沸点差异过大,请用键能大小解释CO2是分子晶体,熔点、沸点高低是由比较微弱的范德华力决定的而与化学键强弱无关,SiO2属原子晶体,其熔点、沸点高低是由强大的共价键决定的.
(4)在一定条件下,Cl-与R2+可形成一种无限长链离 ,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$.
,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$.
(5)A元素能形成组成为Pt(AH3)2Cl2 的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大.
①Q是非极性分子(填“极性”或“非极性”)分子,
②P的结构简式为 ( AH3配体作为一个整体写).
( AH3配体作为一个整体写).
| 元素 | A | B | R | D |
| 相关信息 | 基态原子核外电子占据3个能级且最高能级上有3个电子 | B的单质是最常见半导体材料 | 位于第四周期I B族 | 是非金属元素,其形成的某种单质是电的良导体,有的分子形状似足球 |
(2)A、B,D均可形成多种氢化物,在最常见的三种氢化物中,分子构型为三角锥的氢化物分子式为NH3,任意写出一种中心原子存在sp2、sp3两种杂化类型的物质的结构简式CH2=CH-CH3,与A的常见单质互为等电子体的上述元素的氧化物是CO.
(3)B、D均可形成氧化物,等物质的量的B、D的最高价氧化物中σ键之比为2:1,已知有下列两种数据:
| 键能(kJ/mol) | 熔点(K) | 沸点(K) | |
| BO2 | B-O:452 | 1923 | 2503 |
| DO2 | D=O:615,D-O:348 | 216 | 195 |
(4)在一定条件下,Cl-与R2+可形成一种无限长链离
 ,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$.
,研究表明该离子中每个氯原子最外层均达到8电子稳定结构,有些氯与R之间存在配位键,若该长链离子中含有n个R,则该离子的化学式为$(CuC{l}_{3}{)_{n}}^{n-}$.(5)A元素能形成组成为Pt(AH3)2Cl2 的配合物,该配合物存在两种同分异构体:一种为淡黄色(Q),不具有抗癌作用,在水中的溶解度小;另一种为黄绿色(P),具有抗癌作用,在水中的溶解度较大.
①Q是非极性分子(填“极性”或“非极性”)分子,
②P的结构简式为
 ( AH3配体作为一个整体写).
( AH3配体作为一个整体写).
9.化学与生活密切相关,下列说法正确的是( )
| A. | 凡含有食品添加剂的食物对人体健康均有害 | |
| B. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
7.对于4℃时100mL水中溶解了22.4LHCl气体(标准状况下测得)后形成的溶液,下列说法中正确的是:
( )
( )
| A. | 该溶液物质的量浓度为10moL/L | |
| B. | 所得的溶液的体积为22.5L | |
| C. | 该溶液中溶质的质量分数因溶液的密度未知而无法求得 | |
| D. | 根据题干数据,该溶液物质的量浓度无法求得 |
6.河虾不宜与西红柿同食,主要原因是河虾中含+5价砷,西红柿中含有较多的维生素C,两者同食会产生有毒的+3价砷.据此,下列说法不正确的是( )
0 151806 151814 151820 151824 151830 151832 151836 151842 151844 151850 151856 151860 151862 151866 151872 151874 151880 151884 151886 151890 151892 151896 151898 151900 151901 151902 151904 151905 151906 151908 151910 151914 151916 151920 151922 151926 151932 151934 151940 151944 151946 151950 151956 151962 151964 151970 151974 151976 151982 151986 151992 152000 203614
| A. | 该反应中维生素C作还原剂 | |
| B. | 河虾与其它含维生素C较多蔬菜也不宜同食 | |
| C. | 河虾与西红柿同食发生了氧化还原反应 | |
| D. | 该反应中砷元素被氧化 |
 A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:
A、B、C、D为原子序数依次增大的四种元索,A2-和B+具有相同的电子构型;C、D为同周期元索,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子.回答下列问题:

 .
. .
. .
. .
.